网址:http://m.1010jiajiao.com/timu_id_3702854[举报]
为减少和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.甲醇是一种可再生燃料,它的沸点为64.7℃.有科学家提出绿色构想:把含有CO2的空气或工业尾气通入碳酸钾溶液中,然后再把CO2从溶液中提取出来,经化学反应后得到甲醇,其构想流程如下:(相对原子质量:C-12 O-16 Ca-40 Ba-137)
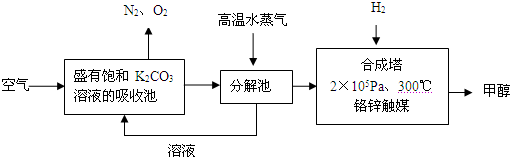
试回答下列问题:
(1)写出分解池中发生反应的化学方程式______.
(2)在2×105Pa、300℃合成塔中,若有CO2与H2反应生成32g甲醇和水,放出49.5kJ的热量,试写出合成塔中发生反应的热化学方程式:_____________.
(3)在合成塔中发生的是放热反应,高温不利于甲醇的生成,合成塔中维持300℃的较高温度的原因可能是______;若要提高甲醇的产率,可采取的措施有(写2条):______、______.
(4)甲醇的一个重要作用是制燃料电池,常用KOH作电解质溶液,负极的电极反应式为:______.
(5)常温常压下,饱和CO2水溶液的pH=5.6,c (H2CO3)=1.5×10-5mol?L-1,若忽略水的电离和H2CO3的二级电离,则H2CO3?HCO3-+H+的平衡常数K=______(计算结果保留2位有效数字,己知10-5.6=2.5×10-6).
(6)某同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积常数分别为4.96×10-9、2.58×10-9,该同学应该选用较合适的试剂是______(填字母).
A.Ba(OH)2溶液 B.Ca(OH)2溶液
C.BaCl2和NaOH混合溶液 D.CaCl2溶液.
查看习题详情和答案>>
| A、1moLH2完全燃烧生成气态水时所放出的热量,叫做氢气的燃烧热 | B、同温、同压下,H2(g)+Cl2(g)=2HCl(g) 在光照和点燃条件下发生的反应,△H一定不同 | C、水的电离平衡常数、化学平衡常数、难溶电解质的溶度积常数等都随温度的升高而增大. | D、对一个正反应吸热的可逆反应来说,升高温度,正反应速率加快,逆反应也速率加快 |
研究化学反应原理对于生产生活是很有意义的。
(1)下列关于醋酸的叙述正确的是 (填写符号)。
a.醋酸俗名冰醋酸,是食醋的主要成分
b.向醋酸溶液中加入一定量NaOH固体,溶液的导电性增强
c.加水稀释醋酸溶液,溶液中的所有离子浓度均减小
d.常温下,醋酸溶液中水的电离程度减小
(2)牙釉质对牙齿起着保护作用,其主要成分为Ca5(PO4)3OH,该物质在水中存在沉淀溶解
平衡,试写出该物质的溶度积常数表达式Kap= 。
(3)钢铁生锈现象随处可见,钢铁的电化腐蚀原理
如图所示:
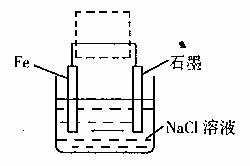
①写出石墨电极的电极反应式 ;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向。
③写出修改后石墨电极的电极反应式 。
查看习题详情和答案>>已知25℃时0.1![]() 醋酸溶液的pH值约为3.向其中加入少量醋酸钠晶体,待晶体溶解后发现溶液pH值增大.对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,增大了
醋酸溶液的pH值约为3.向其中加入少量醋酸钠晶体,待晶体溶解后发现溶液pH值增大.对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,增大了![]() ,因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使
,因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使![]() 减小,因此溶液pH值增大.你认为上述两种解释中________(“甲”或“乙”)正确.
减小,因此溶液pH值增大.你认为上述两种解释中________(“甲”或“乙”)正确.
(1)为了验证上述哪种解释正确,继续做如下实验:向0.1![]() 的醋酸溶液中加入少量下列物质________(填写编号),然后测定溶液的pH值.
的醋酸溶液中加入少量下列物质________(填写编号),然后测定溶液的pH值.
[ ]
A.固体![]()
B.固体![]()
C.气体![]()
D.固体![]()
(2)若________(填“甲”或“乙”)的解释正确,溶液的pH值应________(填“增大”、“减小”或“不变”).
(已知:25℃时,0.1![]() 氨水的电离度为1.3%,0.1
氨水的电离度为1.3%,0.1![]() 醋酸的电离度为1.3%)
醋酸的电离度为1.3%)
|
以下说法错误的是 | |
| [ ] | |
A. |
将pH=4的醋酸稀释后,溶液中所有离子的浓度均减小 |
B. |
pH=11的某物质的水溶液中,对水的电离可能促进也可能是抑制 |
C. |
改变条件使醋酸的电离平衡向右移动,醋酸的电离度可能增大也可能减小 |
D. |
改变条件使醋酸钠溶液中的醋酸根离子浓度增大,溶液的pH可能减小也可能增大 |