摘要:2.常见阴离子的检验 物质 检验方法 OH- 能使① 无色酚酞.② 紫色石蕊.③ 橙色的甲基橙等指示剂分别变为红色.蓝色.黄色. C1- 能与AgNO3溶液反应.生成白色的AgCl沉淀.沉淀不溶于稀硝酸.能溶于氨水.生成. Br- 能与AgNO3溶液反应.生成淡黄色AgBr沉淀.沉淀不溶于稀HNO3. I- ① 能与AgNO3反应.生成黄色AgI沉淀.沉淀不溶于稀HNO3.② I-也能与氯水反应生成I2.使淀粉溶液变蓝 SO42- 能与含Ba2+溶液反应.生成白色BaSO4沉淀.沉淀不溶于硝酸. SO32- ① 浓溶液能与强酸反应.产生无色有刺激性气味的SO2气体.该气体能使品红溶液褪色.② 能与BaCl2溶液反应.生成白色BaSO3沉淀.该沉淀溶于盐酸.生成无色有刺激性气味的SO2气体.注:BaSO3在硝酸中也不溶解.而是转化为BaSO4沉淀.但有NOx放出. S2- 能与Pb(NO3)2或CuSO4溶液反应.生成黑色PbS或CuS沉淀. CO32- 能与BaCl2溶液反应.生成白色的BaCO3沉淀.该沉淀溶于硝酸.生成无色无味能使澄清石灰水变浑浊的CO2气体. HCO3- ① 取含HCO3-盐溶液煮沸.放出无色无味CO2气体.气体能使澄清石灰水变浑浊.或 ② 向HCO3-盐酸溶液里加入稀MgSO4溶液.无现象.加热煮沸.有白色沉淀生成.同时放出CO2气体. PO43- 含PO43-的中性溶液.能与AgNO3反应.生成黄色Ag3PO4沉淀.该沉淀溶于硝酸. NO3- 浓溶液或晶体中加入铜片.浓H2SO4加热.放出红棕色气体.有关反应方程式为:NO3-+H2SO4=HSO4-+HNO3.Cu+4HNO3 Cu(NO3)2+2NO2↑+ 2H2O. 特别提醒:无机物鉴别颜色方面的突破口:
网址:http://m.1010jiajiao.com/timu_id_3702751[举报]
中学化学常见物质A、B、C、D之间存在如下转化关系:A+B-C+D+H2O(没有配平),请按要求填空:
(1)若A为短周期组成的黑色固体物质,与B的浓溶液共热时,产生C、D两种气体.C、D两种气体均能使澄清石灰水变浑浊,则该反应的化学方程式是
A.氯化钡溶液 B.高锰酸钾溶液 C.品红溶液 D.酸化的硝酸钡溶液
向500ml 2mol/L的NaOH溶液中通入0.8mol无色无味的C气体,恰好完全反应,该反应的离子方程式是
(2)若A在水中的溶解度随温度升高而降低,B为短周期非金属单质,D是漂白粉的成分之一.D发生水解反应的离子方程式是
(3)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,受热易分解,分解后生成两种极易溶于水的气体.检验A中阴离子的方法是
查看习题详情和答案>>
(1)若A为短周期组成的黑色固体物质,与B的浓溶液共热时,产生C、D两种气体.C、D两种气体均能使澄清石灰水变浑浊,则该反应的化学方程式是
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
,鉴别这两种气体不能选用的试剂是
| ||
A
A
.A.氯化钡溶液 B.高锰酸钾溶液 C.品红溶液 D.酸化的硝酸钡溶液
向500ml 2mol/L的NaOH溶液中通入0.8mol无色无味的C气体,恰好完全反应,该反应的离子方程式是
4CO2+5OH-=CO32-+3HCO3-+2H2O
4CO2+5OH-=CO32-+3HCO3-+2H2O
.此时溶液中的离子浓度按照由大到小的顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
.(2)若A在水中的溶解度随温度升高而降低,B为短周期非金属单质,D是漂白粉的成分之一.D发生水解反应的离子方程式是
ClO-+H2O?HClO+OH-
ClO-+H2O?HClO+OH-
.(3)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,受热易分解,分解后生成两种极易溶于水的气体.检验A中阴离子的方法是
配成溶液,取少量溶液于试管中,滴加硝酸银溶液产生白色沉淀,再滴加稀硝酸沉淀不溶解
配成溶液,取少量溶液于试管中,滴加硝酸银溶液产生白色沉淀,再滴加稀硝酸沉淀不溶解
(简述操作过程及结论).中学化学中几种常见物质的转化关系如图所示:

已知:B、C、D为常见单质,其中C为气休,B、D为金属;F为常见的强酸;K常温下为气体,且能使品红溶液褪色;将E溶液滴入沸水可制得一种红褐色胶体.
请回答下列问题:
(1)若用B作阳极,D作阴极,A溶液为电解质溶液,通电一段时间后,A溶液的pH
(2)写出反应③的离子方程式
(3)写出检验G溶液中阳离子的方法
(4)实验中保存E溶液时要加入
查看习题详情和答案>>

已知:B、C、D为常见单质,其中C为气休,B、D为金属;F为常见的强酸;K常温下为气体,且能使品红溶液褪色;将E溶液滴入沸水可制得一种红褐色胶体.
请回答下列问题:
(1)若用B作阳极,D作阴极,A溶液为电解质溶液,通电一段时间后,A溶液的pH
不变
不变
(填“变大”、“变小”或“不变”).(2)写出反应③的离子方程式
2Fe3++Cu=2Fe2++Cu2+
2Fe3++Cu=2Fe2++Cu2+
,反应④的化学方程式Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(3)写出检验G溶液中阳离子的方法
取G溶液少许于试管中,滴加KSCN溶液,没明显现象,再加入氯水溶液变成血红色,证明G溶液中含而Fe2+
取G溶液少许于试管中,滴加KSCN溶液,没明显现象,再加入氯水溶液变成血红色,证明G溶液中含而Fe2+
.(4)实验中保存E溶液时要加入
加入适量的稀盐酸
加入适量的稀盐酸
,用必要的文字和离子方程式解释原因Fe3++3H2O?Fe(OH)3+3H+,加盐酸抑制Fe3+的水解
Fe3++3H2O?Fe(OH)3+3H+,加盐酸抑制Fe3+的水解
.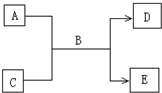 (2009?南充模拟)A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:
(2009?南充模拟)A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:(1)常温下,若A为气态单质,C为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E>D,则:该反应的反应方程式为
Cl2+SO2+2H2O=H2SO4+2HCl
Cl2+SO2+2H2O=H2SO4+2HCl
,检验D中阴离子的方法是先加硝酸酸化无沉淀,再滴加AgNO3溶液有白色沉淀生成,则含Cl-
先加硝酸酸化无沉淀,再滴加AgNO3溶液有白色沉淀生成,则含Cl-
.(2)若A为短周期的金属单质,D为气态单质,C溶液呈强酸性或强碱性时,该反应都能进行.写出反应的离子方程式
2Al+6H+=2Al3++3H2↑
2Al+6H+=2Al3++3H2↑
;2Al+2OH-+H2O=2AlO-+H2↑
2Al+2OH-+H2O=2AlO-+H2↑
.(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的化学式(写两种)
H2SiO3
H2SiO3
、Al ( OH )3
Al ( OH )3
写出生成E的一个离子方程式SiO32-+CO2+H2O=CO32-+H2SiO3↓或 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
SiO32-+CO2+H2O=CO32-+H2SiO3↓或 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
.或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
(10分)下列转化关系中,X、Y是生活中用处广泛的两种金属单质,A、B是氧化物,A呈红棕色,C、D、E是中学常见的三种化合物。分析转化关系回答问题
(1) 请写出反应①的化学方程式:______________
(2) 检验D溶液中问离子的方法是______________;
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式_______;
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制备一种髙效净水剂Y(OH)SO4,已知还原产物为N0,则该反应的化学方程式是_______;
(5)工业上电解熔融的B制取X时,若阳极产生的气体在标准状况下的体积为33.6 m3,则阴极产物的质量为_______kg。
查看习题详情和答案>>
(10分)下列转化关系中,X、Y是生活中用处广泛的两种金属单质,A、B是氧化物,A呈红棕色,C、D、E是中学常见的三种化合物。分析转化关系回答问题
(1) 请写出反应①的化学方程式:______________
(2) 检验D溶液中问离子的方法是______________;
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式_______;
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制备一种髙效净水剂Y(OH)SO4,已知还原产物为N0,则该反应的化学方程式是_______;
(5)工业上电解熔融的B制取X时,若阳极产生的气体在标准状况下的体积为33.6 m3,则阴极产物的质量为_______kg。