网址:http://m.1010jiajiao.com/timu_id_3702055[举报]
实验室需用2mol·L-1氯化钠溶液450 mL,配制时应选用容量瓶的规格和称取氯化钠的质量分别是
A.450 mL,52.7 g B.500 mL,58.5 g
C.450 mL,58.5 g D.500 mL,52.7 g
查看习题详情和答案>>
(7分)“烂版液”是制印刷锌版时,用稀硝酸腐蚀锌版后得到的“废液”。若产生的气体为N2O,稀硝酸腐蚀锌版反应的主要化学方程式是 。“烂版液”的主要成分是 和由自来水带进的Cl-、Fe3+等杂质离子。
在实验室中,由“烂版液”制取ZnSO4?7H2O的过程如下:
① 在“烂版液”中逐渐加入6mol?L-1NaOH溶液,用pH试纸检验,至pH=8为止。
② 过滤后得到Zn(OH)2沉淀,用去离子水多次洗涤沉淀。
③ 用2mol?L-1的硫酸,慢慢将洗净的Zn(OH)2溶解,保持一定的pH,加热煮沸,趁热过滤,滤液即为ZnSO4溶液。
④ 溶液中注入2 mol?L-1的硫酸,使其pH保持为2,将溶液小心加热,冷却后即得到ZnSO4?7H2O晶体。
在操作①中保持pH=8的目的是 。Cl-、NO3-是在操作 中除净的。操作③中加热的目的是 。Fe3+是在操作 中除去的。操作④保持pH=2的目的是 。操作④中所用的主要仪器是 。
查看习题详情和答案>>(1)用不到的仪器是(用字母表示)
A.烧杯 B.200mL容量瓶 C.量筒 D.胶头滴管 E.玻璃棒:F.100mL容量瓶
(2)配制时应称取KOH
(3)实验开始时,需检查容量瓶
(4)下列操作的顺序是(用字母表示)
(5)若用2mol?L-1的KOH溶液润洗容量瓶,实验结果使溶液浓度将
 (1)环境专家认为可以用铝将水中的NO3- 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).
(1)环境专家认为可以用铝将水中的NO3- 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).NO3-+
(2)若4Al(s)+3O2(g)=2Al2O3(s)△H=-a KJ/mol
Fe2O3(s)+
| 3 |
| 2 |
| 3 |
| 2 |
C(s)+O2(g)=CO2(g)△H=-c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式:
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
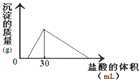
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为