网址:http://m.1010jiajiao.com/timu_id_3694479[举报]
 甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料。已知CH3OH(l)O2(g)=CO(g)+2H2O(g) △Ha=-443.64KJ?mol-1 2CO(g)+O2(g)=2CO2(g)
甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料。已知CH3OH(l)O2(g)=CO(g)+2H2O(g) △Ha=-443.64KJ?mol-1 2CO(g)+O2(g)=2CO2(g)
△Hb=-566.0KJ?mol-1
(1)试写出CH3OH(l)在氧气中完全燃烧生成CO2和H2O(汽)的热化学方程式: ____________________________________________________________________________________________________________
(2)有人认为:在一定条件下,完全可实现由CO2和H2O(汽)来制取CH3OH(l)的反应,从而能缓解能源紧张和温室效应的问题。试通过计算说明,这种反应是否具有可行性?
(3)科研人员新近开发出一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,可使手机连续使用一个月才充一次电,据此回答下列问题:
甲醇在__________极反应;电极反应式为____________________________________________
(4)利用电池可实现电能向化学能转化。某同学设计了一种电解法制取Fe(OH)2的实验装置,通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是_____(填序号)
A. 电源中的a一定为正极,b一定为负极
B. 可以用NaCl作为电解液
C. A、B两端都必须用铁作电极
D. 阴极发生的反应是:2H++2e-→H2↑
查看习题详情和答案>>
| |||||||||||||||||||||||||
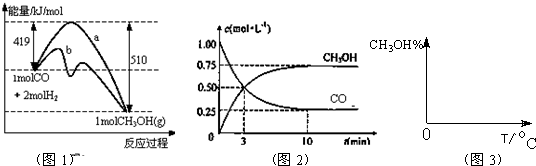
请回答下列问题:
(1)在“图1”中,曲线
(2)下列说法正确的是
A.起始充入的CO为2mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会减小
(3)从反应开始到建立平衡,v(H2)=
(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2).
(5)已知CH3OH(g)+
| 3 |
| 2 |
又知H2O(l)=H2O(g)△H=+44kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式
| 3 |
| 2 |
| 3 |
| 2 |
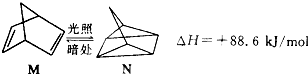
则M、N相比,较稳定的是
(2)已知CH3OH(l)的燃烧热△H=-238.6kJ/mol,CH3OH(l)+
| 1 |
| 2 |
则a
(3)将CH3OH设计成燃料电池,KOH溶液为电解质溶液,则通CH3OH气体的电极为电池的
(4)断裂1mol化学键所需的能量见下表:
| 共价键 | H-N | H-O | N≡N | O=O |
| 断裂1mol化学键所需能量/kJ/mol | 393 | 460 | 941 | 499 |
 (2011?太原二模)现已确认,CO、SO2和NOx的排放是造成大气污染的重要原因.
(2011?太原二模)现已确认,CO、SO2和NOx的排放是造成大气污染的重要原因.(1)用CO2和氢气合成CH3OH具有重要意义,既可以解决环境问题,还可解决能源危机.已知CH3OH具有重要意义,既可以解决环境问题,还可解决能源危机.已知CH3OH、H2的燃烧热分别为-726.5kJ/mol、-285.8kJ/mol,写出工业上用CO2和H2合成CH3OH的热化学方程式:
(2)用铂作电极,一极通入空气,一极通入CH3OH(l),与KOH溶液可组成燃料电池,其负极反应式为
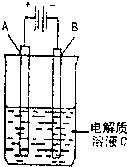
(3)如图是一个电化学装置示意图,用CH3OH-空气燃料电池作此装置的电源.
①如果A为粗铜,B为纯铜,C为CuSO4溶液.该原理的工业生产意义是
②如果A是铂电极,B是石墨电极,C是AgNO3溶液.通电后,若B极增重10.8g,该燃料电池理论上消耗
结果保留两位有效数字)
(4)常温下向1L、0.2mol/L NaOH溶液中通入4.48L(标准状况)的SO2(忽略混合后溶液体积的变化),若测得溶液的pH<7,则溶液中c(SO32-)_
A.c(SO32-)十c(OH-)+c(HSO3-)=c(Na+)+c(H+)
B.c(H2SO3)+c(HSO3-)+c(SO32-)=0.2mol/L
C.c(H2SO3)+c(H+)=c(SO32-)十c(OH-)
D.c(Na+)>c(H+)>c(HSO3-)>c(OH-)
