摘要:35.⑴ ⅠA或第一主族 ⑵ 物理变化 ⑶ NaCl.58.5 ⑷ NaOH+SO3==NaHSO3 . NaHSO3+HCl==NaCl+H2O+SO2 ↑ ⑸ C.D
网址:http://m.1010jiajiao.com/timu_id_3692752[举报]
A、B、C、D、E五种元素原子序数依次增大,除E外均为短周期主族元素,B、C、D同周期,A、D同主族.A的最外层有三个未成对的电子,B是同周期第一电离能最小的元素,C的原子结构示意图为: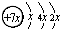 ,E的价层电子排布式为3d64s2.回答下列问题:
,E的价层电子排布式为3d64s2.回答下列问题:
(1)写出下列元素的符号:A
(2)用元素符号表示A、C、D电负性由小到大的顺序
(3)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(4)D的氢化物比A的氢化物的沸点
(5)E元素在周期表的位置是
(6)B、C、D最高价氧化物的晶体类型是分别是
查看习题详情和答案>>
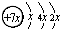 ,E的价层电子排布式为3d64s2.回答下列问题:
,E的价层电子排布式为3d64s2.回答下列问题:(1)写出下列元素的符号:A
N
N
BNa
Na
CSi
Si
DP
P
(2)用元素符号表示A、C、D电负性由小到大的顺序
Si<P<N
Si<P<N
.(3)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
HNO3
HNO3
.(4)D的氢化物比A的氢化物的沸点
低
低
(填“高“或“低“),A的氢化物分子立体构型为三角锥形
三角锥形
.(5)E元素在周期表的位置是
第四周期、Ⅷ族
第四周期、Ⅷ族
.(6)B、C、D最高价氧化物的晶体类型是分别是
离子晶体
离子晶体
、原子晶体
原子晶体
、分子晶体
分子晶体
.[化学--选修物质结构与性质]
已知A、B、C、D、E、F、G位于元素周期表的前四周期,且元素原子序数依次增加,A焰色反应呈黄色;工业常用电解B的熔融的氯化物来制备B,C是一种能被HF和NaOH溶液溶解的单质,D的电负性比磷大,第一电离能却比磷小,E单质是制备漂白液的原料,F能形成红色(或砖红色)和黑色的两种氧化物,G是一种主族金属.
(1)前四周期所有元素中,基态原子中未成对电子与其所在周期数相同的元素有 种.
(2)元素A、B、C分别与氟气化合形成物质X、Y、Z熔点见下表:
解释表中氟化物熔点差异的原因: .
(3)已知常温条件下,极性分子DOE2是一种液态化合物,中心原子D的杂化方式是 .向盛有10mL水的锥形瓶中滴加少量的DOE2溶液,生成两种有刺激性气味的气体.请书写此反应的化学方程式 .
(4)G与氮原子可1:1化合,形成人工合成的新型半导体材料,其晶体结构与单晶硅相似.G原子的价电子排布式为 .在该合成材料中,与同一个G原子相连的N原子构成的空间构型为正四面体.在四种基本晶体类型中,此晶体属于 晶体.
(5)F晶体的堆积方式是 (填堆积名称),其配位数为 . 向F的硫酸盐溶液中滴加氨水直至过量,写出此过程所涉及的两个离子方程式 根据价层电子对互斥理论,预测SO42-的空间构型为 .
查看习题详情和答案>>
已知A、B、C、D、E、F、G位于元素周期表的前四周期,且元素原子序数依次增加,A焰色反应呈黄色;工业常用电解B的熔融的氯化物来制备B,C是一种能被HF和NaOH溶液溶解的单质,D的电负性比磷大,第一电离能却比磷小,E单质是制备漂白液的原料,F能形成红色(或砖红色)和黑色的两种氧化物,G是一种主族金属.
(1)前四周期所有元素中,基态原子中未成对电子与其所在周期数相同的元素有
(2)元素A、B、C分别与氟气化合形成物质X、Y、Z熔点见下表:
| 氟化物 | X | Y | Z |
| 熔点/K | 1266 | 1534 | 183 |
(3)已知常温条件下,极性分子DOE2是一种液态化合物,中心原子D的杂化方式是
(4)G与氮原子可1:1化合,形成人工合成的新型半导体材料,其晶体结构与单晶硅相似.G原子的价电子排布式为
(5)F晶体的堆积方式是
 (2013?绵阳模拟)A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大.其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体.
(2013?绵阳模拟)A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大.其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体.(1)M的基态原子价层电子排布式为
3d24s2
3d24s2
,元素B、D、G的第一电离能由大到时小的顺序是N>O>S
N>O>S
(用元素符号表示).(2)用价层电子对互斥理论预测,GD32-的立体构型是
三角锥型
三角锥型
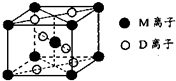
(用文字表述)(3)M与D形成的一种橙红色晶体晶胞结构如图所示,其化学式为
TiO2
TiO2
(用元素符号表示).(4)已知化合物EB结构与单晶硅相似,该物质可由E 的氯化物与NaB3在高温下反应制得,且生成单质B2,该反应化学方程式为
AlCl3+3NaN3═3NaCl+AlN+4N2↑
AlCl3+3NaN3═3NaCl+AlN+4N2↑
,若有8.4gB2生成,则转移电子数为1.204×1023或0.2NA
1.204×1023或0.2NA
. (2011?濮阳二模)A、B、C、D、E五种元素都是36号以前元素,原子序数依次增大,其相关信息如下表
(2011?濮阳二模)A、B、C、D、E五种元素都是36号以前元素,原子序数依次增大,其相关信息如下表| 元素 | 相关信息 |
| A | A的第一电离能低于同周期相邻元素 |
| B | B原子中成对电子数等于未成对电子数的2倍 |
| C | C原子p轨道和s轨道中的电子数相等,与非金属的原子结合时形成共价键 |
| D | D与A、B、C均不同周期,其单质分子中只有一条共价键 |
| E | E在所处周期中电负性最大,且与D是同一主族元素 |
B
B
BC
C
CO
O
DCl
Cl
,EBr
Br
;(2)A与D形成的化合物的化学式为
BCl3
BCl3
,其分子的立体构型是平面正三角形
平面正三角形
,是非极性
非极性
(填“极性”或“非极性”)分子;(3)请比较化合物ED与Cl2、Br2、I2三者沸点由高到低的顺序:
I2
I2
>Br2
Br2
>BrCl
BrCl
>Cl2
Cl2
,其理由是
BrCl与Cl2、Br2、I2结构相似,都能形成分子晶体,相对分子质量越大,分子间作用力越强,沸点越高
BrCl与Cl2、Br2、I2结构相似,都能形成分子晶体,相对分子质量越大,分子间作用力越强,沸点越高
.(4)A的最高价氧化物的水化物(H2AO3)晶体是一种白色片层状结构,层内的H3AO3分子这间有序排列如图.
①在H3AO3分子中,A原子的杂化方式是
sp2
sp2
;②在晶体中,H3AO3分子能形成这种排列方式的原因是
H3BO3分子之间氢原子与氧原子之间存在氢键
H3BO3分子之间氢原子与氧原子之间存在氢键
;③在H3AO3晶体中层与层之间的作用力是
分子间作用力
分子间作用力
,该晶体属于分子
分子
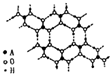
晶体. [化学-选修物质结构与性质]现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元(图形以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同).A、B的晶体类型相同,单质A的同素异形体能与B物质发生置换反应.C、D、E、F含有相同的电子数,且D是阳离子,D与F的组成元素相同.C、E、F的晶体类型相同,由E构成的物质常温下呈液态.
[化学-选修物质结构与性质]现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元(图形以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同).A、B的晶体类型相同,单质A的同素异形体能与B物质发生置换反应.C、D、E、F含有相同的电子数,且D是阳离子,D与F的组成元素相同.C、E、F的晶体类型相同,由E构成的物质常温下呈液态.(1)写出单质A的同素异形体与B物质发生置换反应的化学方程式①
(2)上述六种物质或粒子的组成元素中有三种处于同一周期,请写出这三种元素第一电离能由大到小的顺序
(3)F分子的空间构型是①
(4)C分子的中心原子杂化类型是