网址:http://m.1010jiajiao.com/timu_id_3685525[举报]
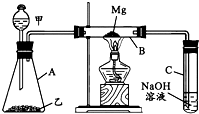 某研究性学习小组认为SiO2、SO2和CO2都是酸性氧化物,化学性质应具有一定的相似性,他们以课本知识“Mg在点燃的条件下可与CO2反应”为基础,设计了如图所示装置进行Mg和SO2反应的实验.据此请回答:
某研究性学习小组认为SiO2、SO2和CO2都是酸性氧化物,化学性质应具有一定的相似性,他们以课本知识“Mg在点燃的条件下可与CO2反应”为基础,设计了如图所示装置进行Mg和SO2反应的实验.据此请回答:(1)若用下列物质中的两种相互混合反应制取SO2,则这两种物质最好是
①10%的H2SO4溶液
②50%的H2SO4溶液
③Na2SO3固体
④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式
| ||
| ||
| ||
| ||
(3)你认为该装置是否有不足之处?如果有,请说明之.答:
(4)有同学认为,B管中的生成物中含有MgS,请你设计实验方案加以证明.答:
①2Mg+O2
| 点燃 |
| 点燃 |
| 点燃 |
④Mg+H2O
| 点燃 |
| 点燃 |
完成下列填空:
现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2).实验装置如下(部分夹持仪器省略).
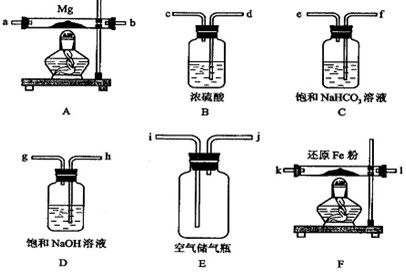
(1)装置F的作用是
(2)请设计一个实验,验证产物是氮化镁:
镁在电子工业中利用镁制取硅的反应为:2Mg+SiO2
| △ |
| △ |
Mg2Si遇盐酸迅速反应生成SiH4(硅烷).SiH4在常温下是一种不稳定、易分解的气体.
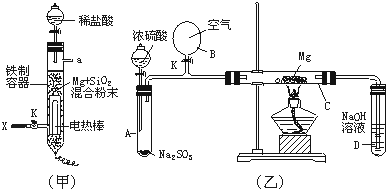
(3)图(甲)是进行Mg与SiO2反应的实验装置.由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气.X气体应选用①CO2、②N2、③H2中的
(4)图(乙)所示装置进行的实验如下:先关闭K,使A中反应进行;加热玻璃管C,可观察到C管中发出耀眼白光,产生白烟,管壁上附着有淡黄色物质.实验完成后,将C管中固体全部加入盐酸中,有臭鸡蛋气味的气体生成.C中的Mg应放在不锈钢垫片上而不能直接接触管壁,这是因为
 查看习题详情和答案>>
查看习题详情和答案>>
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)冶炼铜的反应为:
8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
除去Al3+的离子方程式是 。
(3)为验证炉渣中含有FeO,先将炉渣用稀酸溶解,再在酸性条件下加入适当的氧化剂。(提供的试剂:稀盐酸、稀硫酸、KSCN溶液、酸性KMnO4溶液、NaOH溶液、碘水)
所选试剂为 、 ,证明炉渣中含有FeO的实验现象为 。
(4)配平上述反应的离子方程式(氧化性物质依据你的选择填入[ ])
Fe2++ H++ [ ] → Fe3++ [ ]+ H2O
(5)如果证明炉渣中是否含有FeO,将炉渣溶于稀硝酸,每含有1molFeO,可产生气体的体积是 L(标准状况,假设硝酸的还原产物只有NO)。
(6)Fe2O3可以作为染料,也可进一步制得净水剂Fe2(SO4)3, Fe2(SO4)3的净水原理是 (用相应的方程式表示)。
查看习题详情和答案>>
 某研究性学习小组认为SiO2、SO2和CO2都是酸性氧化物,化学性质应具有一定的相似性,他们以课本知识“Mg在点燃的条件下可与CO2反应”为基础,设计了如图所示装置进行Mg和SO2反应的实验.据此请回答:
某研究性学习小组认为SiO2、SO2和CO2都是酸性氧化物,化学性质应具有一定的相似性,他们以课本知识“Mg在点燃的条件下可与CO2反应”为基础,设计了如图所示装置进行Mg和SO2反应的实验.据此请回答: 8Cu +4FeO+2Fe2O3+16SO2,若CuFeS2,中Fe的化合价为+2价,反应中被还原的元素是______。
8Cu +4FeO+2Fe2O3+16SO2,若CuFeS2,中Fe的化合价为+2价,反应中被还原的元素是______。