摘要:5.质量分数-时间图象 例7.对于可逆反应mApC反应过程中. 其他条件不变时.产物D的质量分数D%与温度T或压强p的关系如图9所示.请判断下列说法正确的是( ). A.降温.化学平衡向正反应方向移动 B.使用催化剂可使D%有所增加 C.化学方程式中气体的化学计量数m<p+q D.B的颗粒越小.正反应速率越快.有利于平衡向正反应方向移动 解析:这类图象的解题方法是“先拐先平 .即曲线先折拐的首先达到平衡.以此判断温度或压强的高低.再依据外界条件对平衡的影响确定答案.答案 A.C 图7 曲线图 以上是常见的几种平衡图象及一般解题思路.具体问题要注意综合.灵活地运用. 例8.反应2X2Z.在不同温度(T1和T 2)及压强(p1和p2)下.产物Z的物质的量(n2)与反应时间(t)的关系如图10所示.下述判断正确的是( ). A.T1<T2.p1<p2 B.T1<T2.p1>p2 C.T1>T2.p1>p2 D.T1>T2.p1<p2 图8 曲线图 解析:该题要综合运用“定一论二 .“先拐先平 解题,也可依据“定一论二 和外界条件对化学平衡的影响解题.答案:C . 知能训练
网址:http://m.1010jiajiao.com/timu_id_3684641[举报]
 向一个容积为2L的恒温容密闭容器中通入2molA,发生如下反应:
向一个容积为2L的恒温容密闭容器中通入2molA,发生如下反应:2A(g)?-2B(g)+C(?),5min后反应达到平衡,测得平衡后容器内的压强和开始时相同,B在混合气体中所占的体积分数是80%,反应吸收的热量是56Kj.请填写下列空白:
(1)该温度下,下列叙述可以说明该反应已达平衡状态的是
①V(A)=v(B)②v正(A)=v逆(B)
③A、B的物质的量相等④C的物质的量不再变化
⑤混合气体的平均相对分子质量不再变化⑥混合气体的密度不再变化
⑦混合气体的总物质的量不再变化
(2)该温度下,此反应的化学平衡常数为
(3)该反应的热化学反应方程式为
已知:该条件下产物C不为液态).
(4)在该温度下的速率时间图象中,假设第6min时将容器体积从2L变为1L,请在右图中补画出该反应的速率随时间的变化情况.
(5)保持恒温容,在原平衡体系中再充入3molA,平衡将
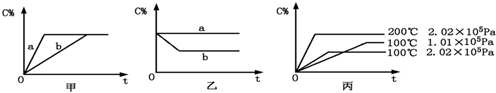
现有下列可逆反应:A(g)+B(g)=xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如图:
请根据图象回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况(填字母,下同);
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性气体后的情况,则 曲线表示恒温恒容的情况;
(3)根据丙图可以判断该可逆反应的正反应是 热反应(填“吸”或“放”);
(4)化学计量数x的值 (填取值范围);判断的依据是 .
查看习题详情和答案>>

请根据图象回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性气体后的情况,则
(3)根据丙图可以判断该可逆反应的正反应是
(4)化学计量数x的值
随着人类社会的发展,氮氧化物(Nox)已成为大气中的主要气态污染物之一.
(1)超音速飞机排放的尾气是平流层中NO的主要来源.它们破坏臭氧层的机理为:
①O3
O+O2
②NO→NO2+O2
③NO2+O→NO+O2
上述反应的总反应式为
(2)汽车尾气中含有NOx、CO和碳氢化合物等.
①尾气净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如图1所示,尾气净化过程中发生的总反应化学方程式:
②NOx和碳氢化合物在阳光照射下发生光化学反应产生二次污染物的现象,称为“光化学烟雾”.有学者对某城市.天中光化学烟雾的变化情况进行测定,实验结果如图2.由图象可知,二次污染物有
③测定汽车尾气中Nox的方法之一是用3%的H2O2溶液吸收尾气中的NOx生成HNO3,再用NaOH标准溶液滴定HNO3.若要测定标准状况下尾气中NOx的体积分数,所需的数据有
A.所测尾气的总体积 B.两种氮氧化物的体积比
C.NaOH标准溶液的物质的量浓度 D.所消耗NaOH标准溶液的体积
E.从滴定开始到指示剂变色所需的时间
(3)硝酸工业尾气中的NOx可用纯碱溶液吸收,有关的化学反应为:
2NO2+Na2O=NaNO3+CO2
NO+NO2+Na2CO3=2NaNO3+CO2
现用0.5L 2mol/L的纯碱溶液恰好吸收一定量硝酸工业尾气中的NOx,吸收液质量增加44g(设C02全部排出).则NO2和NO的体积比为
查看习题详情和答案>>
(1)超音速飞机排放的尾气是平流层中NO的主要来源.它们破坏臭氧层的机理为:
①O3
| 光 |
②NO→NO2+O2
③NO2+O→NO+O2
上述反应的总反应式为
2O3
3O2
| ||
2O3
3O2
,其中
| ||
NO
NO
是催化剂.
(2)汽车尾气中含有NOx、CO和碳氢化合物等.
①尾气净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如图1所示,尾气净化过程中发生的总反应化学方程式:
2NO+O2+4CO
4CO2+N2
| ||
2NO+O2+4CO
4CO2+N2
.
| ||
②NOx和碳氢化合物在阳光照射下发生光化学反应产生二次污染物的现象,称为“光化学烟雾”.有学者对某城市.天中光化学烟雾的变化情况进行测定,实验结果如图2.由图象可知,二次污染物有
醛和O3
醛和O3
等,醛和O3的峰值出现在14:00左右的主要原因是此时日光强烈,光化学反应速率最快
此时日光强烈,光化学反应速率最快
;③测定汽车尾气中Nox的方法之一是用3%的H2O2溶液吸收尾气中的NOx生成HNO3,再用NaOH标准溶液滴定HNO3.若要测定标准状况下尾气中NOx的体积分数,所需的数据有
ACD
ACD
(选填序号).A.所测尾气的总体积 B.两种氮氧化物的体积比
C.NaOH标准溶液的物质的量浓度 D.所消耗NaOH标准溶液的体积
E.从滴定开始到指示剂变色所需的时间
(3)硝酸工业尾气中的NOx可用纯碱溶液吸收,有关的化学反应为:
2NO2+Na2O=NaNO3+CO2
NO+NO2+Na2CO3=2NaNO3+CO2
现用0.5L 2mol/L的纯碱溶液恰好吸收一定量硝酸工业尾气中的NOx,吸收液质量增加44g(设C02全部排出).则NO2和NO的体积比为
7:1
7:1
.现有下列可逆反应:A(g)+B(g)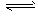 xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
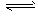 xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图: 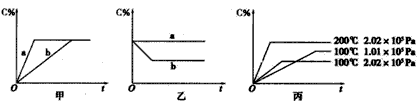
请根据图象回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则____曲线表示无催化剂时的情况(填字母,下同);
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性气体后的情况,则____曲线表示恒温恒容的情况;
(3)根据丙图可以判断该可逆反应的正反应是____热反应(填“吸”或“放”);
(4)化学计量数x的值___(填取值范围);判断的依据是____。
查看习题详情和答案>>
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则____曲线表示无催化剂时的情况(填字母,下同);
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性气体后的情况,则____曲线表示恒温恒容的情况;
(3)根据丙图可以判断该可逆反应的正反应是____热反应(填“吸”或“放”);
(4)化学计量数x的值___(填取值范围);判断的依据是____。
随着人类社会的发展,氮氧化物(NOx)已成为大气中的主要气态污染物之一。
(1)超音速飞机排放的尾气是平流层中NOx的主要来源。它们破坏臭氧层的机理为:
①O3 O+O2 ②NO+O3→NO2+O2 ③NO2+O→NO+O2
O+O2 ②NO+O3→NO2+O2 ③NO2+O→NO+O2
上述反应的总反应式为____________________,其中________是催化剂。
(2)汽车尾气中含有NOx、CO和碳氢化合物等。
①汽车尾气净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如图所示
(1)超音速飞机排放的尾气是平流层中NOx的主要来源。它们破坏臭氧层的机理为:
①O3
 O+O2 ②NO+O3→NO2+O2 ③NO2+O→NO+O2
O+O2 ②NO+O3→NO2+O2 ③NO2+O→NO+O2 上述反应的总反应式为____________________,其中________是催化剂。
(2)汽车尾气中含有NOx、CO和碳氢化合物等。
①汽车尾气净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如图所示

尾气净化装置中发生的总反应的化学方程式为________________。
②NOx和碳氢化合物在阳光照射下发生光化学反应产生二次污染物的现象,称为“光化学烟雾”。有学者对某城市一天中光化学烟雾的变化情况进行测定,实验结果如图所示。由图象可知,二次污染物有
________等,醛和O3的峰值出现在14∶00左右的主要原因是__________________________。
②NOx和碳氢化合物在阳光照射下发生光化学反应产生二次污染物的现象,称为“光化学烟雾”。有学者对某城市一天中光化学烟雾的变化情况进行测定,实验结果如图所示。由图象可知,二次污染物有
________等,醛和O3的峰值出现在14∶00左右的主要原因是__________________________。

③测定汽车尾气中NOx的方法之一是用3%的H2O2溶液吸收尾气中的NOx生成HNO3,再用NaOH标准溶液滴定HNO3。若要测定标准状况下尾气中NOx的体积分数,所需的数据有________(选填序号)。
A.所测尾气的总体积
B.两种氮氧化物的体积比
C.NaOH标准溶液的物质的量浓度
D.所消耗NaOH标准溶液的体积
E.从滴定开始到指示剂变色所需的时间
(3)硝酸工业尾气中的NOx可用纯碱溶液吸收,有关的化学反应为:
2NO2+Na2CO3==NaNO2+NaNO3+CO2
NO+NO2+Na2CO3==2NaNO2+CO2
现用0.5 L 2 mol/L的纯碱溶液恰好吸收一定量硝酸工业尾气中的NOx,吸收液质量增加44 g(设CO2全部排出)。则NO2和NO的体积比为________。
查看习题详情和答案>>
A.所测尾气的总体积
B.两种氮氧化物的体积比
C.NaOH标准溶液的物质的量浓度
D.所消耗NaOH标准溶液的体积
E.从滴定开始到指示剂变色所需的时间
(3)硝酸工业尾气中的NOx可用纯碱溶液吸收,有关的化学反应为:
2NO2+Na2CO3==NaNO2+NaNO3+CO2
NO+NO2+Na2CO3==2NaNO2+CO2
现用0.5 L 2 mol/L的纯碱溶液恰好吸收一定量硝酸工业尾气中的NOx,吸收液质量增加44 g(设CO2全部排出)。则NO2和NO的体积比为________。