摘要:燃料电池 负极:2H2+4OH--2e-=4H2O 正极:O2+2H2O+2e-=4OH- 电池的总反应为:2H2 + O2 = 2H2O 疑难点拨
网址:http://m.1010jiajiao.com/timu_id_3684334[举报]
 (1)阿波罗宇宙飞船使用的是碱性氢氧燃料电池,负极贮存的是氢气,正极贮存的是氧气,电解质是NaOH溶液.请写出该反应发生的电极反应式.
(1)阿波罗宇宙飞船使用的是碱性氢氧燃料电池,负极贮存的是氢气,正极贮存的是氧气,电解质是NaOH溶液.请写出该反应发生的电极反应式.正极:
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
;负极:2H2+4OH--4e-=4H2O
2H2+4OH--4e-=4H2O
;总反应:2H2+O2=2H2O
2H2+O2=2H2O
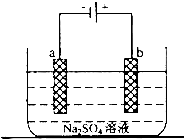
.(2)如图为直流电源电解稀Na2SO4水溶液的装置.通电后在石墨电极a和b附近分别滴加一滴石蕊溶液.
①a电极上的电极反应式为
2H++2e-=H2↑
2H++2e-=H2↑
;②在b极附近观察到的现象是
有气泡冒出,溶液显红色
有气泡冒出,溶液显红色
;③电解一段时间后,加入适量
H2O
H2O
可以使电解质溶液恢复到原来的浓度.氢氧燃料电池是将氢和氧分别通入电池,穿过浸入20%~40%的KOH溶液的多孔碳电极,其电极反应为:2H2 +4OH- - 2e-=4H2O和O2 +2H2O+ 2e-=4OH-,则下列叙述正确的是
[ ]
A.通入H2的一极是正极,通入O2的一极是负极
B.通入O2的一极是正极,通入H2的一极是负极
C.电池工作一段时间后,电解质溶液的pH增大
D.电池在工作时,负极区附近的pH增大
查看习题详情和答案>>
B.通入O2的一极是正极,通入H2的一极是负极
C.电池工作一段时间后,电解质溶液的pH增大
D.电池在工作时,负极区附近的pH增大
(1)我国首创的海洋电池,总反应为:4Al+3O2+6H2O═4Al(OH)3,负极为
(2)航天技术使用氢氧电池具有高能、轻便,不污染优点,氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式均可表示为:2H2+O2═2H2O.酸式氢氧燃料电池的电解质是酸,其负极反应为:2H2-4e-═4H+,则正极反应为
(3)蓄电池Pb+PbO2+2H2SO4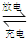 2PbSO4+2H2O放电时,正极电极反应式
2PbSO4+2H2O放电时,正极电极反应式
查看习题详情和答案>>
Al
Al
,负极发生氧化
氧化
反应(填“氧化”或“还原”),负极反应Al-3e-=Al3+
Al-3e-=Al3+
;正极为铂网,电流
电流
(填“电子”或“电流”)从铂极流出;海水为电解质溶液,海水中的Na+移向正极
正极
(填“正极”或“负极”).(2)航天技术使用氢氧电池具有高能、轻便,不污染优点,氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式均可表示为:2H2+O2═2H2O.酸式氢氧燃料电池的电解质是酸,其负极反应为:2H2-4e-═4H+,则正极反应为
O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
;碱式氢氧燃料电池的电解质是碱,其正极反应表示为:O2+2H2O+4e-═4OH-,则负极反应为:2H2-4e-+4OH-=4H2O
2H2-4e-+4OH-=4H2O
.(3)蓄电池Pb+PbO2+2H2SO4
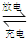 2PbSO4+2H2O放电时,正极电极反应式
2PbSO4+2H2O放电时,正极电极反应式PbO2+2e-+SO42-+4H+=PbSO4+2H2O
PbO2+2e-+SO42-+4H+=PbSO4+2H2O
,当电路中通过0.5mol电子时,消耗H2SO4的物质的量0.5mol
0.5mol
,负极增重24
24
g. 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电.(1)a是
负
负
极,电极反应式是2H2-4e-+4OH-=4H2O(或H2-2e-+2OH-=2H2O)
2H2-4e-+4OH-=4H2O(或H2-2e-+2OH-=2H2O)
;b是正
正
极.电极反应式是O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
.(2)飞船上宇航员的生活用水由燃料电池提供.若为飞行员提供了360kg的水,则电路中通过了
4×104
4×104
mol的电子. 我国“神舟”号宇宙飞船成功发射并回收,是我国航天史上的里程碑. 飞船上使用的氢氧燃料电池是一种新型的化学电源,它具有高能、轻便、不污染环境的特点.这种燃料电池的构造如右图所示,两个电极均由多空性碳制成,通入的气体由空隙逸出并在电极表面放电.
我国“神舟”号宇宙飞船成功发射并回收,是我国航天史上的里程碑. 飞船上使用的氢氧燃料电池是一种新型的化学电源,它具有高能、轻便、不污染环境的特点.这种燃料电池的构造如右图所示,两个电极均由多空性碳制成,通入的气体由空隙逸出并在电极表面放电.a极是
负
负
极,b极是正
正
极,写出电极反应式a:负极:2H2-4e-+4OH-=4H2O;(或H2-2e-+2OH-=2H2O)
负极:2H2-4e-+4OH-=4H2O;(或H2-2e-+2OH-=2H2O)
;b:
正极:O2+4e-+2H2O=4OH-
正极:O2+4e-+2H2O=4OH-
;总反应式:
2H2+O2=2H2O
2H2+O2=2H2O
.