网址:http://m.1010jiajiao.com/timu_id_3684309[举报]
在1L密闭容器中发生反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-Q kJ?mol-1(Q>O),容器内部分物质的物质的量浓度如下表:
|
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 5.8 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 8.8 | 3.2 | 5.2 | 6.7 |
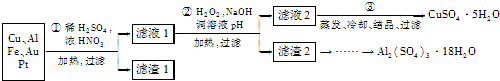
(1)第①步操作前需将金属混合物进行粉碎,其目的是
(2)某学生认为用H2O2代替浓HNO3更好,理由是
请写出Cu溶于H2O2与稀硫酸混合溶液的离子方程式:
(3)第②步中应将溶液pH调至
(4)由滤渣2制取Al2(SO4)3?18H2O,探究小组设计了两种方案:
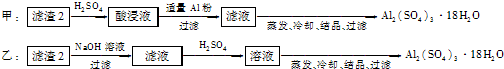
你认为
(5)为了测定硫酸铜晶体的纯度,某同学准确称取4.0g样品溶于水配成100mL溶液,取10mL溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.100 0mol?L-1Na2S2O3标准溶液滴定至终点,共消耗14.00mL Na2S2O3标准溶液.上述过程中反应的离子方程式如下:
2Cu2++4I-═2CuI(白色)↓+I2S2O
2- 3 |
2- 6 |
①样品中硫酸铜晶体的质量分数为
②另一位同学提出通过测定样品中硫酸根离子的量也可求得硫酸铜晶体的纯度,其他同学认为此方案不可行,理由是
(1)①该反应的熵变△S
②升高温度,反应的平衡常数K值减小,则该反应的焓变△H
(2)若其他条件不变,下列关系图错误的是
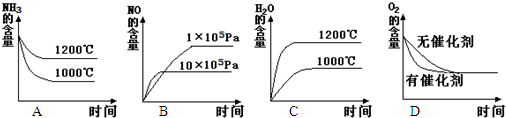
(3)在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表:
| 时间/浓度/(mol?L-1) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第 2min | 3.2 | 4.5 4.5 |
0.8 | 1.2 |
| 第 4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第 6min | 2.0 | 3.0 | 2.0 | 3.0 |
②反应在第2min时改变了条件,改变的条件可能是
工业上可以从电解铜的阳极泥中提取很多重要物质,其工艺流程如下:
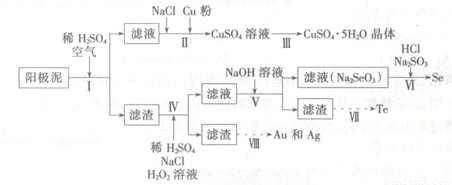
已知:①阳极泥的主要化学成分,如表1所示
表一
主要成份 | Cu??? Ag???? Au????? Se???? Te |
百分含量/% | 23.4??? 12.1???? 0.9???? 6.7???? 3.1 |
②温度和硫酸浓度对阳极泥中各组分浸出率的影响,如表2所示
表二
| 固定浸出温度 |
|
| 固定H2SO4浓度
|
H2SO4浓度 mol/L | 浸出率/% |
| 浸出温度/℃ | 浸出率/% |
Cu? Ag? Au? Se? Te |
| Cu? Ag? Au? Se? Te | ||
4 | 95.1 4.67? <0.2? 0.83 8.93 |
| 30 | 87.1 4.58? <0.2 0.08 6.83 |
3 | 94.5 4.65? <0.2? 0.28 6.90 |
| 40 | 94.5 4.65? <0.2? 0.28 6.90 |
2 | 78.1 2.65? <0.2? 0.05 2.85 |
| 50 | 96.1 5.90? <0.2? 0.64 8.73 |
(1)步骤I的主要目的为浸出铜,此过程中发生的主要反应的化学方程式为____________分析表2数据,可知步骤I最适合的条件为??????????????????? 。
(2)步骤Ⅱ中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为____。
(3)步骤Ⅲ的操作方法为????????????????????? 。
(4)步骤Ⅳ中,反应温度为75℃。加入H2O2溶液的作用为?????????????????? ;此过程中H2O2溶液的添加量要远远高于理论值,原因为?????????????????? 。
(5)步骤Ⅵ中所发生反应的化学方程式为?????? ???????????????? 。
(6)步骤Ⅶ中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为 ???? 。
(7)步骤Ⅷ中得到的Au和Ag混合物可以用____进行分离(填选项字母)。
A.稀硝酸 ?? B.浓盐酸? ?? C.浓氢氡化钠溶液? ?? D.王水
查看习题详情和答案>>
(共6分)实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:

|
实验次数 |
起始温度t1/℃ |
终止温度t2/℃ |
|
|
盐酸 |
NaOH溶液 |
||
|
1 |
20.2 |
20.3 |
23.7 |
|
2 |
20.3 |
20.5 |
23.8 |
|
3 |
21.5 |
21.6 |
24.9 |
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是 。
(2)在操作正确的前提下,提高中和热测定准确性的关键是 。
(3)根据上表中所测数据进行计算,则该实验测得的中和热ΔH= [盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。如用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将 (填“偏大”、“偏小”、 “不变”)。
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大
查看习题详情和答案>>