网址:http://m.1010jiajiao.com/timu_id_3684288[举报]


(2)已知白磷在氧气中燃烧可能生成两种固态氧化物物(P4O6与 P4O10),3.1g白磷在3.2g氧气中恰好完全反应,放出热量a kJ。计算白磷的燃烧热为ΔH=________(第(1)小题中的ΔH以-b kJ/mol带入计算)
(3)已知白磷与红磷互为同素异形体,它们各自的主要理化性质如下:


能源是人类生存和发展的重要支撑因素.请回答以下有关能源的问题:
(1)人类历史进程的各个阶段,如按石器时代、铁器时代、蒸汽时代、电气时代划分,各时代主要的动力源分别是:______、_______、________、________.
(2)人类所使用的能量绝大部分来源于太阳能.捕获太阳能的生物主要为绿色植物.绿色植物能够通过光合作用把太阳能转化为化学能,光合作用的总反应式是_________________.光合作用释放的氧气来自于参加反应的哪种物质?_________.
(3)煤、石油、天然气、水能及生物能等是多年来大规模使用的能源,被称为______能源.而核能、地热、海洋能、沼气以及现在又有新的利用方式的太阳能、风能等都被称为______能源.煤、石油、天然气等能源以热的形式供给人们需要的能量.试以它们各自的主要成分C、
 为代表,写出它们燃烧过程的化学方程式.指出它们质量相同时,哪一种燃料对环境造成的负面影响(产生温室效应)最小.
为代表,写出它们燃烧过程的化学方程式.指出它们质量相同时,哪一种燃料对环境造成的负面影响(产生温室效应)最小.
能源是人类生存和发展的重要支撑因素.请回答以下有关能源的问题:
(1)人类历史进程的各个阶段,如按石器时代、铁器时代、蒸汽时代、电气时代划分,各时代主要的动力源分别是:______、_______、________、________.
(2)人类所使用的能量绝大部分来源于太阳能.捕获太阳能的生物主要为绿色植物.绿色植物能够通过光合作用把太阳能转化为化学能,光合作用的总反应式是_________________.光合作用释放的氧气来自于参加反应的哪种物质?_________.
(3)煤、石油、天然气、水能及生物能等是多年来大规模使用的能源,被称为______能源.而核能、地热、海洋能、沼气以及现在又有新的利用方式的太阳能、风能等都被称为______能源.煤、石油、天然气等能源以热的形式供给人们需要的能量.试以它们各自的主要成分C、
 为代表,写出它们燃烧过程的化学方程式.指出它们质量相同时,哪一种燃料对环境造成的负面影响(产生温室效应)最小.
为代表,写出它们燃烧过程的化学方程式.指出它们质量相同时,哪一种燃料对环境造成的负面影响(产生温室效应)最小.
(1)脱硝.利用甲烷催化还原NOx:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1 CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ?mol-1甲烷直接将NO2还原为N2的热化学方程式为
(2)脱碳.将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H3
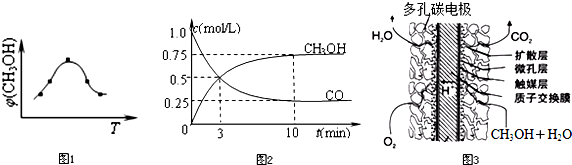
①取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线(见图1),则上述CO2转化为甲醇反应的△H3
②在一恒温恒容密闭容器中充入1mol CO2和3mol H2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如图2所示.下列说法正确的是
A.第10min后,向该容器中再充入1mol CO2和3mol H2,则再次达到平衡时c(CH3OH)=1.5mol/L
B.达到平衡时,氢气的转化率为0.75
C.0~10分钟内,氢气的平均反应速率为0.075mol/(L?min)
D.该温度下,反应的平衡常数的值为3/16
E.升高温度将使n(CH3OH)/n(CO2)增大
③直接甲醇燃料电池结构如图3所示.其工作时负极电极反应式可表示为
(3)脱硫.某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.设烟气中的SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为
(1)脱硝.利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ?mol-1
甲烷直接将NO2还原为N2的热化学方程式为
(2)脱碳.将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H3<0
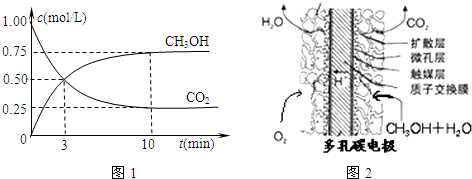
①在一恒温恒容密闭容器中充入1mol CO2和3mol H2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如图1所示.下列说法正确的是
A.第10min后,向该容器中再充入1mol CO2和3mol H2,则再次达到平衡时c(CH3OH)=1.5mol?L-1
B.0~10min内,氢气的平均反应速率为0.075mol/(L?min)
C.达到平衡时,氢气的转化率为75%
D.该温度下,反应的平衡常数的值为
| 3 |
| 16 |
E.升高温度将使
| n(CH3OH) |
| n(CO2) |
②甲醇燃料电池结构如图2所示.其工作时正极的电极反应式可表示为:
(3)脱硫.某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表为: