网址:http://m.1010jiajiao.com/timu_id_3682145[举报]
硬质玻璃管是化学实验中经常使用的一种仪器,分析下列实验(固定装置及尾气处理过程均略去)并回答:
(1)如图所示,通入C12—段时间后,观察A、B、C三个棉球的变化,并补充完成下表所示的实验报告。
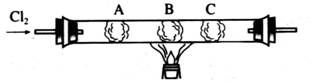
|
实验内容 |
实验现象[来源:Zxxk.Com] |
解释或结论 |
|
|
棉 球 |
棉球上滴加试剂 |
||
|
A |
KBr溶液 |
棉球变为___________色 |
化学方程式:__________ |
|
B |
_____溶液 |
棉球变为棕黄色 |
离子方程式:__________ |
|
C |
淀粉溶液 |
①棉球变为蓝色; ②待试管冷却后,在B、C之间的玻璃壁上有_____ 色固体产生 |
②的原因:__________ |
(2)实验室里,氯气通常用浓盐酸和二氧化锰在加热的条件下制取,该反应的化学方程
式为______________________________,此外还可以用高锰酸钾、氯酸钾等氧化剂与浓盐酸在常温下反应制取。某化学课外活动小组用如图所示的装置制取氯气并模拟盐酸工业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸)。
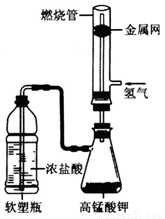
实验过程如下:
步骤一:先通入氢气,验纯后点燃;
步骤二:待氢气稳定燃烧后,挤压软塑瓶,将浓盐酸加入锥形瓶中,氢气持续安静燃烧。
请回答:
①步骤二完成后,火焰的颜色由淡蓝色变为__________色,燃烧管的上方可观察到_____现象;
②先通氢气并点燃,再通氯气的原因是_______________
③采用外管通氢气、内管通氯气的目的是____________________。
查看习题详情和答案>>
硬质玻璃管是化学实验中经常使用的一种仪器,分析下列实验(固定装置及尾气处理过程均略去)并回答:
(1)如图所示,通入C12—段时间后,观察A、B、C三个棉球的变化,并补充完成下表所示的实验报告。
| 实验内容 | 实验现象 | 解释或结论 | |
| 棉 球 | 棉球上滴加试剂 | ||
| A | KBr溶液 | 棉球变为___________色 | 化学方程式:__________ |
| B | _____溶液 | 棉球变为棕黄色 | 离子方程式:__________ |
| C | 淀粉溶液 | ①棉球变为蓝色; ②待试管冷却后,在B、C之间的玻璃壁上有_____ 色固体产生 | ②的原因:__________ |
(2)实验室里,氯气通常用浓盐酸和二氧化锰在加热的条件下制取,该反应的化学方程
式为______________________________,此外还可以用高锰酸钾、氯酸钾等氧化剂与浓盐酸在常温下反应制取。某化学课外活动小组用如图所示的装置制取氯气并模拟盐酸工业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸)。
实验过程如下:
步骤一:先通入氢气,验纯后点燃;
步骤二:待氢气稳定燃烧后,挤压软塑瓶,将浓盐酸加入锥形瓶中,氢气持续安静燃烧。
请回答:
①步骤二完成后,火焰的颜色由淡蓝色变为__________色,燃烧管的上方可观察到_____现象;
②先通氢气并点燃,再通氯气的原因是_______________
③采用外管通氢气、内管通氯气的目的是____________________。
查看习题详情和答案>>
查阅资料 HClO Ka=3.0×10-8,HNO2 Ka=4.6×10-4,HCN Ka=4.93×10-10
探究1.在小烧杯中加入20mL0.1mol/LFeCl3,用pH计测量溶液的pH.在另一只小烧杯中加入5mL0.1mol/LFeCl3溶液,加蒸馏水稀释至50mL,用pH计测量该溶液的pH.将探究得到的结论填写在下面的空格中.
探究2.在A.B两支试管中分别加入等体积0.1mol/LFe2(SO4)3溶液.将A试管在酒精灯火焰上加热到沸腾,B试管保持室温,推测A.B两试管中所盛分散系的颜色的差别.将探究得到的结论填写在下面的空格中.
探究3.取A.B两只小烧杯,在A杯中加入20mL蒸馏水,在B杯中加入20mL10mol/L的HCl,再分别向两只小烧杯中投入2.0gFeCl3固体,用玻璃棒搅拌使固体溶解.A烧杯出现浑浊,B烧杯为澄清溶液.将探究得到的结论及该结论的应用之一填写在下面的空格中.
探究4.取三支试管,分别加入10mL0.1mol/LNaCN.NaClO.NaNO2溶液,用pH测三种盐溶液的pH.推测三种盐溶液pH的相对大小.将探究得到的结论填写在下面的空格中. 回答下列问题
(1)以上四个探究的探究课题是
(2)请将该小组每个探究所得到的结论(有的还要填写结论的应用)填在对应的空格中.
探究1
探究2
探究3
应用举例
探究4

限选试剂:浓硫酸、1.0mol/LHNO3、1.0mol/L盐酸、1.0mol/LNaOH、3% H2O2、0.1mol/LKI、0,1mol/LCuSO4、20% KSCN、澄清石灰水、氧化铜、蒸馏水.
(1)若实验中,观察到B、F中溶液均变浑浊,则E中的现象是
(2)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3.验证固体产物中钾元素存在的方法是
(3)固体产物中铁元素存在形式的探究.
提出合理假设:假设1:
设计实验方案证明你的假设(不要在答题卷上作答)
实验过程
根据上述实验方案进行实验.在答题卷上填写实验步骤、预期现象与结论中的空格.
| 实验步骤 | 预期现象与结论 |
| 步骤1:取适量固体产物于试管中,加入足量蒸馏水,充分振荡使碳酸钾完全溶解.分离不溶固体与溶液,用蒸馏水充分洗涤不溶固体. | 固体产物部分溶解. |
| 步骤2:向试管中加入适量 CuSO4 CuSO4 溶液,再加入少量不溶固体,充分振荡. |
(1)若溶液颜色及加入的不溶固体无明显变化,则假设 2 2 成立.(2)若溶液颜色明显改变,且有 暗红 暗红 色固体生成,则证明有铁单质 铁单质 存在 |
| 步骤3:继续步骤2中的(2),进行固液分离,用蒸馏水洗涤固体至洗涤液无色.取少量固体于试管中,滴加过量 HCl HCl ,静置,取上层清液,滴加适量KSCN KSCN ,充分振荡后滴加H2O2 H2O2 . |
结合步骤2中的(2): (1)若溶液基本无色,则假设 1 1 成立(2)若溶液呈血红色,则假设 3 3 成立 |