摘要: 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑
网址:http://m.1010jiajiao.com/timu_id_3679925[举报]
由铜、锌和稀盐酸组成的原电池中,铜是
查看习题详情和答案>>
正
正
极,发生还原
还原
反应,电极反应式是2H++2e-=H2↑
2H++2e-=H2↑
;锌是负
负
极,发生氧化
氧化
反应,电极反应式是Zn-2e-=Zn2+
Zn-2e-=Zn2+
. (思维拓展题)某研究学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:
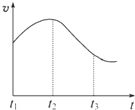
(思维拓展题)某研究学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:实验一、把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示:
实验二、把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气量减少.
实验三、将不纯的锌片与稀盐酸反应,发现反应速率加快.
实验四、在盐酸中滴入几滴CuCl2溶液,同样生成氢气速率加快.
问题:
(1)试分析实验一中t1~t2速率变化的主要原因是
纯锌与稀盐酸反应,放出热量,温度升高
纯锌与稀盐酸反应,放出热量,温度升高
,t2~t3速率变化的主要原因是随着反应进行c(H+)降低
随着反应进行c(H+)降低
.(2)实验二放出氢气量减少的原因是
锌片与FeCl3反应,导致与盐酸反应的锌的质量减少
锌片与FeCl3反应,导致与盐酸反应的锌的质量减少
.(3)某同学认为实验三和四反应速率加快原因,均因为原电池的存在,你认为是否正确,若不正确,说明原因.若正确写出原电池的电解质溶液、正、负极材料及电极反应.
| 负极材料 | 正极材料 | 负极反应式 | 正极反应式 | 电解质溶液 | |
| 实验三 | Zn | 杂质 | Zn-2e-=Zn2+ | 2H++2e-=H2↑ | 盐酸 |
| 实验四 | Zn | Cu | Zn-2e-=Zn2+ | 2H++2e-=H2↑ | 盐酸 |
| 负极材料 | 正极材料 | 负极反应式 | 正极反应式 | 电解质溶液 | |
| 实验三 | Zn | 杂质 | Zn-2e-=Zn2+ | 2H++2e-=H2↑ | 盐酸 |
| 实验四 | Zn | Cu | Zn-2e-=Zn2+ | 2H++2e-=H2↑ | 盐酸 |
(1)某化学反应,设反应物总能量为E1,生成物总能量为E2.若E1>E2,则该反应为
(2)用锌片、铜片和稀盐酸组成的原电池,正极的电极反应是
查看习题详情和答案>>
放
放
热反应,该反应的能量转化是 化学能转化为热能化学能转化为热能
化学能转化为热能
.(2)用锌片、铜片和稀盐酸组成的原电池,正极的电极反应是
2H++2e-=H2↑;
2H++2e-=H2↑;
,负极的电极反应是Zn-2e-=Zn2+;
Zn-2e-=Zn2+;
,原电池反应是Zn+2H+-=Zn2++H2↑
Zn+2H+-=Zn2++H2↑
.(1)用锌片、铜片和稀盐酸组成的原电池,正极的电极反应式为
(2)选用下列试剂和仪器设计一个原电池.画出装置图.标明原电池的正极、负极、电解质溶液,并写出正极、负极的电极反应.
试剂:铜片、铁片、银片、镁条、硫酸铜溶液、硝酸银溶液.
仪器:烧杯、导线、铁夹(若还需其它仪器可自己补充)
查看习题详情和答案>>
2H++2e-=H2↑
2H++2e-=H2↑
,负极的电极反应式为Zn-2e-=Zn2+
Zn-2e-=Zn2+
,原电池的总反应是Zn+2H+=Zn2++H2↑
Zn+2H+=Zn2++H2↑
;当有6.5g锌溶解时,则在标准状况下,放出的氢气的体积为2.24L
2.24L
,转移的电子数为0.2
0.2
摩尔,溶液的酸性减弱
减弱
(填“增强”或“减弱”).(2)选用下列试剂和仪器设计一个原电池.画出装置图.标明原电池的正极、负极、电解质溶液,并写出正极、负极的电极反应.
试剂:铜片、铁片、银片、镁条、硫酸铜溶液、硝酸银溶液.
仪器:烧杯、导线、铁夹(若还需其它仪器可自己补充)