网址:http://m.1010jiajiao.com/timu_id_3678151[举报]
在2 L密闭容器中进行反应:mX(g)+nY(g) ![]() pZ(g)+qQ(g),式中m、n、p、q为物质系数。在0 min~3 min 内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为物质系数。在0 min~3 min 内,各物质物质的量的变化如下表所示:

已知2 min内 v(Q)=0.075 mol·L-1·min-1,且 v(z):v(Y)=1:2
(1)试确定以下物质的相关量:起始时n(Y)=________,n(Q)=_________。
(2)方程式中m =______,n =______, p=______,q=_______。
(3)用Z表示2 min内的反应速率_____________。
(4)2 min末Q的转化率为_____________。
(5)试判断在2 min内v(正)______v(逆)(填“>”、“<”或“=”),在2 min末~3 min末v(正)_____ v(逆)(填“>”、“<”或“=”)。
查看习题详情和答案>>
| |||||||||||||||||||||||||||||||||||||
煤的气化是高效、清洁地利用煤炭的重要途径之一.
(1)在25℃、101 kPa时,H2与O2化合生成1 mol H2O(g)放出241.8 kJ的热量,其热化学方程式为________.
又知:①C(s)+O2(g)=CO2(g); ΔH=-393.5 kJ/mol
②CO(g)+1/2 O2(g)=CO2(g); ΔH=-283.0 kJ/mol
焦炭与水蒸气反应是将固体煤变为气体燃料的方法,C(s)+H2O(g)=CO(g)+H2(g);ΔH=________kJ/mol.
(2)CO可以与H2O(g)进一步发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g);ΔH<0在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,在800℃时达到平衡状态,K=1.0.
CO2(g)+H2(g);ΔH<0在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,在800℃时达到平衡状态,K=1.0.
①该反应的平衡常数表达式为________.
②平衡时,甲容器中CO的转化率是________;
容器中CO的转化率;乙________甲;丙________甲.(填“>”、“=”或“<”)
③丙容器中,通过改变温度,使CO的平衡转化率升高,则温度________(填“升高”或“降低”).
(1)合成碳酸镁晶须的步骤如下:
步骤1.配制0.5mol?L-1MgSO4溶液和0.5mol?L-1NH4HCO3溶液.
步骤2.量取500mL NH4HCO3溶液于1 000mL四口烧瓶中,开启搅拌器.温度控制在50℃.
步骤3.将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,用氨水调节溶液pH到9.5.
步骤4.放置1h后,过滤,洗涤干净.
步骤5.在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3?nH2O n=1~5).
①步骤2控制温度在50℃,较好的加热方法是
②步骤3生成MgCO3?nH2O沉淀的离子方程式为
⑧步骤4检验沉淀已经洗涤干净的方法是
(2)测定合成的MgCO3?nH2O中的n值.
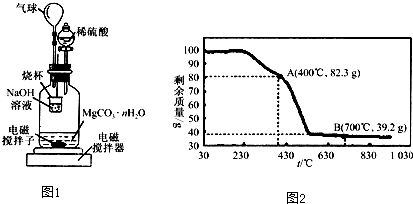
称量1.000g碳酸镁晶须,放入图所示的广口瓶中,加入水,滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5h,反应后期将温度升到30℃,最后,烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次.
①图中气球的作用是
②上述反应后期要升温到30℃,主要目的是
③设3次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为
| (1-84a) |
| 18a |
| (1-84a) |
| 18a |
(3)称取100g上述晶须产品进行热重分析,热重曲线如图2,则该条件下合成的晶须中,n=
 皮江法炼镁工艺原理
皮江法炼镁工艺原理皮江法生产金属镁是以煅烧白云石为原料、硅铁为还原剂、萤石为催化剂,进行计量配料.粉磨后压制成球,称为球团.将球团装入还原罐中,加热到1200℃,内部抽真空至13.3Pa或更高,则产生镁蒸气.镁蒸气在还原罐前端的冷凝器中形成结晶镁,亦称粗镁.再经熔剂精炼,产生商品镁锭,即精镁.
皮江法炼镁生产工序
(1)白云石煅烧:将白云石在回转窑或竖窑中加热至1100~1200℃,烧成煅白(MgO?CaO).
(2)配料制球:以煅白、硅铁粉和萤石粉计量配料、粉磨,然后压制成球.
(3)还原:将料球在还原罐中加热至1200±10℃,在13.3Pa或更高真空条件下,保持8~10小时,氧化镁还原成镁蒸气,冷凝后成为粗镁.
(4)精炼铸锭:将粗镁加热熔化,在约710℃高温下,用溶剂精炼后,铸成镁锭,亦称精镁.
(5)酸洗:将镁锭用硫酸或硝酸清洗表面,除去表面夹杂,使表面美观.
(注:白云石:CaMg(CO3)2 萤石:CaF)
(1)白云石在回转窑或竖窑中煅烧产生的
(2)在还原罐中发生反应的化学方程式为
(3)还原罐抽成真空的目的是
(4)从环保角度考虑,精镁酸洗用
(5)取经酸洗干燥过的镁4.8克,与足量的盐酸反应完全后,得氢气0.402克,则镁中的杂质可能是
A.Zn B.Fe C.Al
若镁仅含上述一种金属杂质,则镁中杂质的质量分数为
(6)皮江法炼镁尽管比融盐电解法有优点,但是它也有一定的缺点,试举出皮江法炼镁一个缺点