网址:http://m.1010jiajiao.com/timu_id_3678016[举报]
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层.
①请写出基态镍原子的核外电子排布式
②NiO、FeO的晶体结构类型均与氯化钠相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
③Ni、Fe、Co等金属都能与CO反应形成配合物,Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于
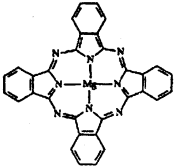
(2)金属酞菁配合物在硅太阳能电池中有重要作用,一种金属镁酞菁配合物的结构如下图,请在下图中用箭头表示出配位键.
(3)CO与N2互为等电子体.CO的总键能大于N2的总键能,但CO比N2容易参加化学反应.根据下表数据,说明CO比N2活泼的原因是
| A-B | A=B | A≡B | ||
| CO | 键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 键能差值(kJ?mol-1) | 441.2 273 | |||
| N2 | 键能(kJ?mol-1) | 154.8 | 418.3 | 941.7 |
| 键能差值(kJ?mol-1) | 263.6 523.3 | |||
 【物质结构与性质】
【物质结构与性质】我国部分城市灰霾天占全年一半,引起灰霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3,有机颗粒物及扬尘等.通过测定灰霾中锌等重金属的含量,可知目前造成我国灰霾天气主要是交通污染.
(1)Zn2+在基态时核外电子排布式为
(2)SO42-的空间构型是
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOX、O3,CH2=CH-CHO,HCOOH,CH3COOONO2(PAN)等二次污染物.
①下列说法正确的是
a.N20结构式可表示为N=N=O
b.O3分子呈直线形
c.CH2=CH-CHO分子中碳原子均采用sp2杂化
d.相同压强下,HCOOH沸点比CH30CH3高,说明前者是极性分子,后者是非极性分子
②1mol PAN中含σ键数目为
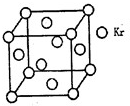
(4)测定大气中PM2.5的浓度方法之一是β一射线吸收法,β一射线放射源可用85Kr,已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则
| m | n |


(2)配位化学创始人维尔纳发现,将各位1mol的CoCl3?6NH3(黄色),CoCl3?5NH3(紫红色),CoCl3?4NH3(绿色),CoCl3?4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,立即沉淀的氯化银分别为3mol,2mol,1mol.和1mol,已知上述配合物中配离子的配位数均为6,请根据实验事实用配合物的形式写出他们的化学式.COCl3?5NH3
(1)O、Si、N元素的电负性由大到小的顺序是
(2)A为短周期金属元素,依据下表数据,写出A的基态原子的轨道表示式
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
(4)H-C≡C-COOH分子内含有
(5)CO可以与金属铁形成配合物分子Fe(CO)5,Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)═Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
⑴O、Si、N元素的电负性由大到小的顺序是____________________。C60和金刚石都是碳的同素异形体,二者中熔点较高的是____________。
⑵A为短周期金属元素,依据下表数据,A的基态原子的轨道表示式为
________________________________。
|
电离能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
|
A |
932 |
1821 |
15390 |
21771 |
⑶过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道的电子排布有关。一般地,若为d0或d10排布时,无颜色;若为d1~d9排布时,有颜色;如[Cu(H2O)4]2+显蓝色。据此判断25号元素Mn形成的络合离子[Mn(H2O)6]2+_____(填“有”或“无”)颜色。
⑷H-C≡C-COOH分子内含有的σ键、π键的个数依次为_______________,其中碳原子的杂化方式为___________________。
⑸CO可以与金属铁形成配合物分子Fe(CO)5。Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键的类型是______________。
⑹W元素的原子的M能层为全充满状态,且核外的未成对电子只有一个,W晶体中微粒的堆积方式是下图中 (选填“甲”、“乙”或“丙”);若W晶体中一个晶胞的边长为a cm,则W晶体的密度为 (写出含a的表达式,用NA表示阿伏加德罗常数)。



甲 乙 丙
查看习题详情和答案>>