摘要:⑴P(s)+Cl2(g)===PCl3(g),ΔH=-306kJ·mol-1. ⑵PCl5(g)===PCl3(g)+Cl2(g),ΔH=93kJ·mol-1.25%,大于. ⑶两步反应均为放热反应.降低温度有利于提高产率.防止产物分解. ⑷-399kJ·mol-1,等于. ⑸PCl5+4H2O===H3PO4+5HCl.
网址:http://m.1010jiajiao.com/timu_id_3669567[举报]
请你回答下列问题:
(1)攀枝花地区是我国钒钛磁铁矿的主要成矿带,钒矿资源较多,居世界第3位,钒(V)元素原子的价电子排布图为: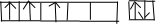
 .钛元素的基态原子的简化电子排布式
.钛元素的基态原子的简化电子排布式
(2)配合物[Cr(NH3)5SO4]Br的中心离子的符号为
(3)有下列四种无机含氧酸:①H3PO4 ②HClO3 ③H3BO3 根据无机含氧酸的酸性规律,将三种无机含氧酸按酸性强弱顺序是
(4)有下列八种物质:①CaCl2晶体 ②干冰 ③NaOH晶体 ④NH4Cl晶体⑤金刚石 ⑥金刚砂晶体.其中含有配位键的离子晶体是
(5)s轨道与s轨道重叠形成的共价键可用符号表示为:δs-s,p轨道与p轨道以“头碰头”方式重叠形成的共价键可用符号δp-p,则H2O分子含有的共价键用符号表示为
查看习题详情和答案>>
(1)攀枝花地区是我国钒钛磁铁矿的主要成矿带,钒矿资源较多,居世界第3位,钒(V)元素原子的价电子排布图为:


[Ar]3d34s2
[Ar]3d34s2
;(2)配合物[Cr(NH3)5SO4]Br的中心离子的符号为
Cr 3+
Cr 3+
,配位数6
6
.(3)有下列四种无机含氧酸:①H3PO4 ②HClO3 ③H3BO3 根据无机含氧酸的酸性规律,将三种无机含氧酸按酸性强弱顺序是
②①③
②①③
.(4)有下列八种物质:①CaCl2晶体 ②干冰 ③NaOH晶体 ④NH4Cl晶体⑤金刚石 ⑥金刚砂晶体.其中含有配位键的离子晶体是
④
④
;属于分子晶体的是②
②
,含有非极性共价键的原子晶体是⑤
⑤
.(5)s轨道与s轨道重叠形成的共价键可用符号表示为:δs-s,p轨道与p轨道以“头碰头”方式重叠形成的共价键可用符号δp-p,则H2O分子含有的共价键用符号表示为
δs-p
δs-p
.Cl2分子含有的共价键用符号表示为δp-p
δp-p
.下列各组物质中,因反应条件、用量、浓度等不同而发生不同化学反应的是( )
①C与O2 ②P与Cl2 ③Fe与S④Na与O2 ⑤CO2与NaOH溶液 ⑥Cu与硝酸 ⑦AgNO3溶液与氨水⑧AlCl3溶液与氨水 ⑨NaAlO2与盐酸 ⑩Na2CO3与盐酸.
①C与O2 ②P与Cl2 ③Fe与S④Na与O2 ⑤CO2与NaOH溶液 ⑥Cu与硝酸 ⑦AgNO3溶液与氨水⑧AlCl3溶液与氨水 ⑨NaAlO2与盐酸 ⑩Na2CO3与盐酸.
查看习题详情和答案>>
红磷P(s)和Cl2发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)根据图回答下列问题.
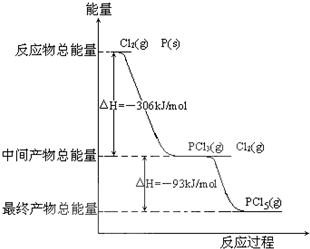
(1)P和Cl2反应生成PCl3的热化学方程式:
(2)PCl5分解生成PCl3和Cl2的热化学方程式:
(3)P和Cl2分两步反应生成1mol PCl5的△H3=
查看习题详情和答案>>

(1)P和Cl2反应生成PCl3的热化学方程式:
P(s)+
Cl2(g)=PCl3(g)△H=-306kJ?mol-1;
| 3 |
| 2 |
P(s)+
Cl2(g)=PCl3(g)△H=-306kJ?mol-1;
;| 3 |
| 2 |
(2)PCl5分解生成PCl3和Cl2的热化学方程式:
PCl5(g)=PCl3(g)+Cl2(g)△H=+93 kJ/mol;
PCl5(g)=PCl3(g)+Cl2(g)△H=+93 kJ/mol;
;温度T1时,在密闭容器中加入0.8mol PCl5,反应达到平衡时还剩余0.6mol PCl5,其分解率α1等于25%
25%
(3)P和Cl2分两步反应生成1mol PCl5的△H3=
-399kJ?mol-1;
-399kJ?mol-1;
;P和Cl2一步反应生成1mol PCl5的△H4等于
等于
△H3(填“大于”,“小于”或“等于”).aX、bY、cZ、dW、eQ为五种原子序数依次增大的短周期元素,Z为地壳中含量最高的金属元素,W与X、Q相邻,W与X具有相同的价电子数,d=2a,3b=d+e.W与Y形成的化合物A的浓溶液在空气中长期放置发生反应,生成物之一B与X与Y1:1组成的化合物C的结构和化学性质相似,其溶液显黄色.回答下列问题:
(1)W元素在周期表中的位置

(2)Q的单质与Y与W形成化合物的溶液反应,有浅黄色沉淀生成,用离子方程式表示原因
(3)W离子与Z离子在溶液中
(4)写出制取Z的化学方程式:
(5)Z与P原子形成P4Z3分子中各原子最外层均已达8电子结构,则一个P4Z3分子中含有共价键总数为
查看习题详情和答案>>
(1)W元素在周期表中的位置
第三周期第VIA族
第三周期第VIA族
化合物B的电子式

(2)Q的单质与Y与W形成化合物的溶液反应,有浅黄色沉淀生成,用离子方程式表示原因
Cl2+S2-═2Cl-+S↓
Cl2+S2-═2Cl-+S↓
.反应后溶液的pH减小
减小
(填“增大”、“不变”或“减小”)(3)W离子与Z离子在溶液中
不能
不能
共存(填能、不能).请用化学用语简要说明原因2Al3++3S2-+6H2O═2Al(OH)3↓+3H2S↑.
2Al3++3S2-+6H2O═2Al(OH)3↓+3H2S↑.
(4)写出制取Z的化学方程式:
2Al2O3
4Al+3O2↑
| ||
2Al2O3
4Al+3O2↑
.
| ||
(5)Z与P原子形成P4Z3分子中各原子最外层均已达8电子结构,则一个P4Z3分子中含有共价键总数为
12
12
个.红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5 (g).反应过程和能量关系如图所示(图中的△H表示生成l mol产物的数据).

根据上图回答下列问题:
(1)PCl5分解成PCl3和Cl2的热化学方程式是
(2)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5原因是
(3)P和Cl2分两步反应生成1mol PCl5的△H3=
查看习题详情和答案>>

根据上图回答下列问题:
(1)PCl5分解成PCl3和Cl2的热化学方程式是
PCl5(g)═PCl3(g)+Cl2(g)△H=+93kJ/lmol
PCl5(g)═PCl3(g)+Cl2(g)△H=+93kJ/lmol
.(2)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5原因是
两步反应均为放热反应,降温有利于提高产率,防止产物分解
两步反应均为放热反应,降温有利于提高产率,防止产物分解
.(3)P和Cl2分两步反应生成1mol PCl5的△H3=
-399kJ/mol
-399kJ/mol
,P和Cl2一步反应生成1mol PCl5的△H4等于
等于
△H3(填“大于”、“小于”或“等于”).简述原因:根据盖斯定律:磷和氯气化学反应不管是一步完成,还是分步完成,其化学反应的焓变是一定的
根据盖斯定律:磷和氯气化学反应不管是一步完成,还是分步完成,其化学反应的焓变是一定的
.