网址:http://m.1010jiajiao.com/timu_id_3653439[举报]
“物质结构与性质”模块(10分)
请回答下列问题:
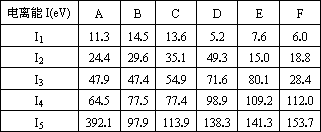
(1)N、AI、Si、Zn四种元素中,有一种元素的电离能数据如下:

(2)则该元素是__①___(填写元素符号)。Zn原子的电子排布式是__②__。Ce的最高价氯化物分子式是_ __③___。该元素可能的性质或应用有__④___。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
关于化合物  ,下列叙述正确的有 ⑤ 。
,下列叙述正确的有 ⑤ 。
A.分子间可形成氢键
B.分子中既有极性键又有非极性键
C.分子中有7个 键和1个
键和1个 键
键
D.该分子在水中的溶解度大于2-丁烯
(4)NaF的熔点 ⑥  的熔点(填>、<或=),其原因是 ⑦
的熔点(填>、<或=),其原因是 ⑦
查看习题详情和答案>>
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有一种为金属,X的核外电子排布式为nsnnpn,Z的最外层电子数是其电子层数的2倍, Y原子与Z原子的最外层电子数之和为9,且Y和W单质都可与烧碱溶液反应,请回答以下问题:
(1)Y、Z、W的原子半径由大到小的顺序是________________(填元素符号)
(2)XZ2的电子式是________________,空间结构为________________,形成晶体时属于________________晶体。
(3)Y的价电子排布式是________________,工业上生产单质Y的原理是________________(用化学反应方程式表示)
(4)试用勒夏特列原理解释用饱和食盐水收集W单质的原理________________。
查看习题详情和答案>>(A)“物质结构与性质”课程模块
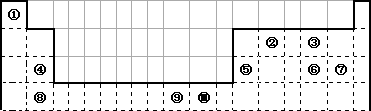
下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于ds区的元素是___________ (填编号)。
(2)表中元素①的2个原子与元素③的2个原子形成的分子中元素③的杂化类型是________;③和⑦形成的常见化合物的化学键类型是___________。
(3)元素⑧的外围电子排布式为___________,该元素原子中未成对电子数为___________。
(4)在周期表中位于对角线的元素的性质也有一定的相似性。试写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_________________________________________________。
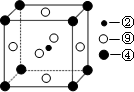
(5)在1 183 K以下,元素⑨形成如图甲所示基本结构单元的晶体;1 183 K以上,转变为图乙所示基本结构单元的晶体。

在1 183 K以下的晶体中,与元素⑨的原子等距离且最近的原子数为___________;在1 183 K以上的晶体中,与元素⑨原子等距离且最近的原子数为___________。
(B)“实验化学”课程模块
已知亚甲基蓝其氧化型呈蓝色,还原型呈无色,其转化关系式为:

氧化型(蓝色)+ne-![]() 还原型(无色)。
还原型(无色)。
奇妙的“蓝瓶子”实验就是利用上述原理,其装置如图甲。
某校化学兴趣小组用图甲装置进行下述实验:
①在250 mL锥形瓶中,依次加入
②塞紧橡皮塞,关闭活塞a、b,静置,溶液变为无色;
③打开活塞、振荡,溶液又变为蓝色;
④关闭活塞、静置,溶液又变为无色;
⑤以上步骤③④可重复多次。
请回答下列问题:
(1)若塞紧图甲中锥形瓶塞,并打开导管活塞a、b,从___________(填“左”或“右”)导管口通入足量氦气后,再关闭活塞a、b并振荡,溶液__________(填“能”或“不能”)由无色变为蓝色。
(2)如图乙所示:某学生将起初配得的蓝色溶液分装在A、B两支试管中,A试管充满溶液,B中有少量溶液,塞上橡皮塞静置片刻,两溶液均显无色。若再同时振荡A、B试管,溶液显蓝色的是___________试管。
(3)上述转化过程中葡萄糖的作用是_______________,亚甲基蓝的作用是______________。
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为______________。
(5)该实验中③④操作___________(填“能”或“不能”)无限次重复进行,理由是____________。
查看习题详情和答案>>
| |||||||||||||||||||||||||||||||
请回答下列问题:
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
| 电离能 I1 I2 I3 I4 … |
| In/kJ.mol-1 578 1817 2745 11578 … |
(2)基态锗(Ge)原子的电子排布式是
A.是一种活泼的金属元素 B.其电负性大于硫 C.其单质可作为半导体材料 D.其最高价氯化物的沸点低于其溴化物的沸点
(3)关于化合物
 ,下列叙述正确的有
,下列叙述正确的有A.分子间可形成氢键 B.分子中既有极性键又有非极性键 C.分子中有7个σ键和1个π键 D.该分子在水中的溶解度大于2-丁烯
(4)NaF的熔点
 的熔点(填>、=或<),其原因是
的熔点(填>、=或<),其原因是