网址:http://m.1010jiajiao.com/timu_id_3633985[举报]
硫、氮及其化合物与人类的生活有着密切关系
ⅠNO分子因污染空气而臭名昭著.近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究的热点,NO亦被称为“明星分子”.请回答下列问题.
(1)NO的危害在于______(填标号).
A.破坏臭氧层 B.高温下能使一些金属氧化
C.造成酸雨 D.与人体血红蛋白结合
(2)在含Cu+离子的酶的活化中心中,亚硝酸根离子可转化为NO,写出Cu+和亚硝酸根离子(NO2-)在酸性水溶液中反应的离子方程式:______.
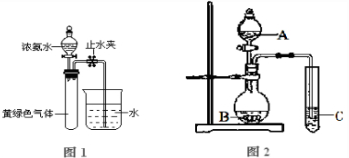
(3)已知NH3和Cl2会发生氧化还原反应,生成N2和NH4Cl.现用如图1所示的装置进行实验,打开分液漏斗的活塞,滴下浓氨水,至不再反应为止;关闭分液漏斗的活塞,待恢复到室温,打开止水夹,试管内液面上升至三分之二处.
①写出实验室制取氨气的化学方程式______.
②试管内发生反应的化学方程式是______.
③试管中发生的反应表明氨气具有______ (填标号).
a、氧化性 b、还原性 c、碱性 d、热不稳定性

Ⅱ(1)将SO2通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,知其中含Cl:35.7%,Cu:64.3%,则SO2在上述反应中的作用是______(填标号).
a.漂白剂 b.氧化剂 c.还原剂
(2)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解.现改用H2O2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式______.
(3)用上图2实验装置可以证明硫、碳、硅三种元素的非金属性强弱.则A、B、C所代表的物质的名称:A______,B______,C______填化学式).
查看习题详情和答案>>
ⅠNO分子因污染空气而臭名昭著.近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究的热点,NO亦被称为“明星分子”.请回答下列问题.
(1)NO的危害在于
A.破坏臭氧层 B.高温下能使一些金属氧化
C.造成酸雨 D.与人体血红蛋白结合
(2)在含Cu+离子的酶的活化中心中,亚硝酸根离子可转化为NO,写出Cu+和亚硝酸根离子(NO2-)在酸性水溶液中反应的离子方程式:
(3)已知NH3和Cl2会发生氧化还原反应,生成N2和NH4Cl.现用如图1所示的装置进行实验,打开分液漏斗的活塞,滴下浓氨水,至不再反应为止;关闭分液漏斗的活塞,待恢复到室温,打开止水夹,试管内液面上升至三分之二处.
①写出实验室制取氨气的化学方程式
②试管内发生反应的化学方程式是
③试管中发生的反应表明氨气具有
a、氧化性 b、还原性 c、碱性 d、热不稳定性
Ⅱ(1)将SO2通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,知其中含Cl:35.7%,Cu:64.3%,则SO2在上述反应中的作用是
a.漂白剂 b.氧化剂 c.还原剂
(2)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解.现改用H2O2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式
(3)用上图2实验装置可以证明硫、碳、硅三种元素的非金属性强弱.则A、B、C所代表的物质的名称:A
从下列事实所得出的结论或给出的解释正确的是( )
|
| 实验事实 | 结论或解释 |
| ① | 将40 g NaOH溶于1 L蒸馏水中 | 该溶液中溶质的质量分数为3.84%,其物质的量浓度为1 mol·L-1 |
| ② | 向盛有1mL 0.1mol·L-1 AgNO3溶液的试管中滴加0.1mol·L-1 NaCl溶液,至不再有沉淀生成,再向其中滴加 0.1mol·L-1 KI溶液,白色沉淀转化为黄色沉淀。 | 常温下,S(AgCl) < S(AgI) |
| ③ | Mg(OH)2难溶于水但可溶于NH4Cl溶液 | NH4Cl水解显酸性,Mg(OH)2与H+发生反应 |
| ④ | 某盐NaX溶液pH > 7 | 酸HX为弱酸 |
| ⑤ | 向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色 | 说明溶液中一定含有Fe2+ |
| ⑥ | 向盛有浓硝酸的试管中分别加入Al片和Cu片,前者没有明显现象,后者反应剧烈,产生大量红棕色气体 | 还原性Al < Cu |
| ⑦ | BaSO4的水溶液导电性很差 | BaSO4是弱电解质 |
A.①⑤⑥ B.④⑤ C.③④⑥⑦ D.③④⑤⑦
查看习题详情和答案>>
从下列事实所得出的结论或给出的解释正确的是( )
|
|
实验事实 |
结论或解释 |
|
① |
将40 g NaOH溶于1 L蒸馏水中 |
该溶液中溶质的质量分数为3.84%,其物质的量浓度为1 mol·L-1 |
|
② |
向盛有1mL 0.1mol·L-1 AgNO3溶液的试管中滴加0.1mol·L-1 NaCl溶液,至不再有沉淀生成,再向其中滴加 0.1mol·L-1 KI溶液,白色沉淀转化为黄色沉淀。 |
常温下,S(AgCl) < S(AgI) |
|
③ |
Mg(OH)2难溶于水但可溶于NH4Cl溶液 |
NH4Cl水解显酸性,Mg(OH)2与H+发生反应 |
|
④ |
某盐NaX溶液pH > 7 |
酸HX为弱酸 |
|
⑤ |
向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色 |
说明溶液中一定含有Fe2+ |
|
⑥ |
向盛有浓硝酸的试管中分别加入Al片和Cu片,前者没有明显现象,后者反应剧烈,产生大量红棕色气体 |
还原性Al < Cu |
|
⑦ |
BaSO4的水溶液导电性很差 |
BaSO4是弱电解质 |
A.①⑤⑥ B.④⑤ C.③④⑥⑦ D.③④⑤⑦
查看习题详情和答案>>