摘要:6.相等物质的量的短周期金属元素单质A和B.分别加入足量的酸.其中A中加入的是盐酸.B中加入的是稀硫酸.二者完全反应后生成的H2体积分别为VA和VB.并且VA≠VB.若要确定反应生成物中A和B的阳离子电荷数.至少还需要给出的数据有 A.VA和VB的比值B.VA的值或VB的值C.A和B的摩尔质量D.盐酸和稀硫酸物质的量浓度
网址:http://m.1010jiajiao.com/timu_id_286215[举报]
在等物质的量的短周期金属元素单质A和B中,分别加入足量的酸,在A中加入盐酸,在B中加入稀硫酸,反应完全后,生成氢气的体积分别为V(A)和V(B),V(A),V(B)不相等.若要确定反应生成物中A和B的化合价,至少还需知道的数据是________,其中原因是________.
查看习题详情和答案>>有物质的量相等的短周期金属元素单质A和B,在A中加入足量盐酸,在B中加入足量稀硫酸,反应完全后,生成氢气的体积为V1和V2,且V1≠V2,若要确定生成物中A和B的化合价,至少还需要的数据是( )
查看习题详情和答案>>
短周期元素D、E、X、Y、Z原子序数逐渐增大.它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形.回答下列问题:
(1)Y的最高价氧化物的化学式为
(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式
(3)D和Y形成的化合物,其分子的空间构型为
(4)D和X形成的化合物,其化学键类型是
(5)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是
(6)试比较的最高价氧化物熔点的高低并说明理由:
查看习题详情和答案>>
(1)Y的最高价氧化物的化学式为
SO3
SO3
;Z的基态原子电子排布式是1s22s22p63s23p5
1s22s22p63s23p5
.(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式
N2O
N2O
.(3)D和Y形成的化合物,其分子的空间构型为
直线型
直线型
;D原子的轨道杂化方式是sp
sp
.X与Z构成的分子是非极性
非极性
分子(填“极性”或“非极性”)(4)D和X形成的化合物,其化学键类型是
极性共价键
极性共价键
,其晶体类型是原子晶体
原子晶体
;(5)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是
Mg3N2;Mg3N2+8H2O=3Mg(OH)2+2NH3.H2O
Mg3N2;Mg3N2+8H2O=3Mg(OH)2+2NH3.H2O
.(6)试比较的最高价氧化物熔点的高低并说明理由:
最高价氧化物熔点X>Z>E>Y>D,二氧化硅为原子晶体,熔点最高,二氧化碳、五氧化二氮、三氧化硫、七氧化二氯都为分子晶体,相对分子质量越大熔点越高
最高价氧化物熔点X>Z>E>Y>D,二氧化硅为原子晶体,熔点最高,二氧化碳、五氧化二氮、三氧化硫、七氧化二氯都为分子晶体,相对分子质量越大熔点越高
.短周期元素X、Y、Z、W原子序数依次增大.X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中.请回答:
(1)Y在元素周期表中的位置是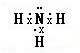
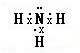 .
.
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈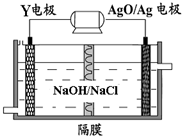
(3)Y-AgO电池是应用广泛的鱼雷电池,其原理如图所示.该电池的负极反应式是
(4)Z和W比较,非金属性较弱的是
a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1mol H-Z或H-W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性.
查看习题详情和答案>>
(1)Y在元素周期表中的位置是
第三周期第ⅢA族
第三周期第ⅢA族
;X氢化物的电子式是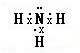
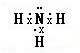
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈
酸
酸
(填“酸”、“碱”或“中”)性,用离子方程式表示其原因是NH4++H2O?NH3?H2O+H+
NH4++H2O?NH3?H2O+H+
.
(3)Y-AgO电池是应用广泛的鱼雷电池,其原理如图所示.该电池的负极反应式是
Al+4OH--3e-=AlO2-+2H2O
Al+4OH--3e-=AlO2-+2H2O
.(4)Z和W比较,非金属性较弱的是
Si
Si
(填元素符号),下列可以验证这一结论的是bcd
bcd
(填序号).a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1mol H-Z或H-W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性.
短周期元素X、Y、Z,X元素最高正价与最低负价的绝对值之差等于4;Y元素的原子半径是短周期中最大的,金属Z的单质能够溶于Y的水溶液.元素X的单质与元素Z的单质在加热条件下反应生成化合物A,A溶于水生成白色沉淀B和气体C,B也能溶于Y的水溶液.C在足量空气中燃烧生成的刺激性气体D是酸雨的主要成分.C被足量Y的水溶液吸收得到无色溶液E.溶液E在空气中长期放置发生反应,生成物之一F与过氧化钠的结构和化学性质相似.
请回答下列问题:
(1)元素X位于周期表中第
(2)F的电子式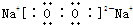
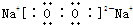
(3)Z与Y水溶液反应的离子方程式为
(4)D与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.该反应的氧化产物为
(5)F的溶液与稀硫酸反应产生的现象为
查看习题详情和答案>>
请回答下列问题:
(1)元素X位于周期表中第
三
三
周期,第VIA
VIA
族.(2)F的电子式
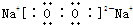
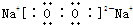
(3)Z与Y水溶液反应的离子方程式为
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.(4)D与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.该反应的氧化产物为
硫酸钠(Na2SO4)
硫酸钠(Na2SO4)
,当生成2mol二氧化氯时,转移电子2
2
mol.(5)F的溶液与稀硫酸反应产生的现象为
溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
.