摘要:强氧化性的:F2.O2.Cl2.Br2,
网址:http://m.1010jiajiao.com/timu_id_284904[举报]
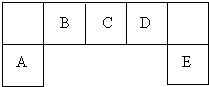 短周期主族元素A、B、C、D、E在元素周期表中的位置如图:请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如图:请回答下列问题:(1)描述D在元素周期表中的位置:
第二周期,ⅥA族
第二周期,ⅥA族
(2)比较A、C、D元素简单离子半径的大小:
N3-
N3-
>O2-
O2-
>Al3+
Al3+
(填元素微粒符号);(3)①写出A的最高价氧化物的水化物与NaOH溶液反应的离子方程式
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
;②用电子式表示B元素的最简单气态氢化物的形成过程
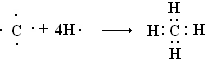
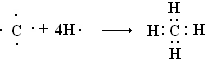
③E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学反应方程式为
8HCl+KClO4
KCl+4Cl2↑+4H2O
| ||
8HCl+KClO4
KCl+4Cl2↑+4H2O
.
| ||
(4)用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式:
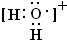
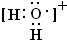
极性共价键
极性共价键
.试写出该阳离子与SO2的水溶液反应的离子方程式SO2+2H2O+=SO42-+4H+
SO2+2H2O+=SO42-+4H+
.(1)常见的染发剂可分为
(2)氯系列消毒剂是目前使用最为广泛的一类消毒剂,其中漂白粉的有效成分为
(3)酸雨有硝酸型酸雨,写出硝酸型酸雨的形成过程的有关方程式:
查看习题详情和答案>>
植物染发剂
植物染发剂
、无机染发剂
无机染发剂
、合成染发剂
合成染发剂
等三大类.(2)氯系列消毒剂是目前使用最为广泛的一类消毒剂,其中漂白粉的有效成分为
Ca(ClO)2
Ca(ClO)2
,在工业上是如何生产漂白粉的写出反应的方程式2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O
2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O
,放在空气会生成有强氧化性的物质试写出反应的方程式Ca(ClO)2+H2O+CO2=2HClO+CaCO3↓
Ca(ClO)2+H2O+CO2=2HClO+CaCO3↓
;氯系列消毒剂在空气中久置会变质为什么:2HClO=2HCl+O2次氯酸分解,无杀菌、漂白性.
2HClO=2HCl+O2次氯酸分解,无杀菌、漂白性.
.(3)酸雨有硝酸型酸雨,写出硝酸型酸雨的形成过程的有关方程式:
N2+O2
2NO
| ||
N2+O2
2NO
,
| ||
2NO+O2=2NO2,3NO2+H2O=2HNO3+NO
2NO+O2=2NO2,3NO2+H2O=2HNO3+NO
,硝酸型酸雨的形成的主要原因是汽车尾气的排放
汽车尾气的排放
;如何减少该类污染?试写出两种方案安装尾气净化装置
安装尾气净化装置
,使用清洁的汽车燃料
使用清洁的汽车燃料
.(2011?天津模拟)下列框表中的A--L中是中学化学中常见的物质,所有物质均由短周期元素组成.已知常温、常压下,C为无色液体,D、E、L均为气体单质,H是一种可溶于盐酸和氢氧化钠溶液的白色固体,J是具有强氧化性的一元弱酸,A--L可发生如下转化:
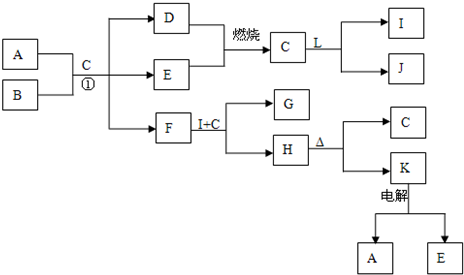
请回答下列问题:
(1)J的电子式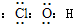
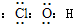
(2)写出C、L反应转化为I和J的离子方程式
(3)H是一种用于治疗胃酸过多的药物的主要成分,其治疗原理用离子方程式表示
(4)写出F与I、C转化为G和H的离子方程式
(5)如果A、B的物质的量之比为2:1,写出①的化学反应方程式
查看习题详情和答案>>

请回答下列问题:
(1)J的电子式
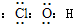
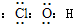
(2)写出C、L反应转化为I和J的离子方程式
Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
(3)H是一种用于治疗胃酸过多的药物的主要成分,其治疗原理用离子方程式表示
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
(4)写出F与I、C转化为G和H的离子方程式
AlO2-+H++H2O=Al(OH)3↓
AlO2-+H++H2O=Al(OH)3↓
(5)如果A、B的物质的量之比为2:1,写出①的化学反应方程式
2Na2O2+4Al+6H2O=4NaAlO2+6H2↑+O2↑
2Na2O2+4Al+6H2O=4NaAlO2+6H2↑+O2↑
.I.如图1是某学生设计的制取和收集某些气体的实验装置(可加热).
(1)该装置在加入反应物前,应首先进行的实验操作是
(2)下列气体的制取中,若用排空气法收集,可使用该装置制备和收集的是(选填编号,下同)
①用Zn与稀盐酸反应制H2
②用CaCO3与稀盐酸反应制CO2
③用固体NaOH和浓氨水制NH3
④用Cu与稀HNO3反应制NO
⑤用MnO2与双氧水反应制O2
⑥浓硫酸与铜片反应制SO2
⑦用MnO2与浓盐酸反应制Cl2
II.某校化学研究性学习小组对浓硫酸与金属锌的反应进行探究.首先按图2组装好实验装置,然后取一定量的浓硫酸与足量Zn充分反应,微热试管A,实验过程中先观察到C、D中均有气泡产生,D中开始出现浑浊,后浑浊消失,随后气泡量逐渐减少,品红溶液褪色,反应较长时间后,C、D中的气泡量又会明显增加.
试回答:
(1)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接
(2)D、E试管中CCl4溶液的作用是防止溶液倒吸,该实验中起到同样作用的装置是
(3)能证明浓硫酸具有强氧化性的实验现象为
(4)反应较长时间后气泡量又会明显增加的原因是
(5)D中浑浊消失的离子方程式为
查看习题详情和答案>>

(1)该装置在加入反应物前,应首先进行的实验操作是
检查装置气密性
检查装置气密性
.(2)下列气体的制取中,若用排空气法收集,可使用该装置制备和收集的是(选填编号,下同)
①③
①③
若用排水法收集(集气瓶中充满水),可使用该装置制备和收集的是①④⑤
①④⑤
.①用Zn与稀盐酸反应制H2
②用CaCO3与稀盐酸反应制CO2
③用固体NaOH和浓氨水制NH3
④用Cu与稀HNO3反应制NO
⑤用MnO2与双氧水反应制O2
⑥浓硫酸与铜片反应制SO2
⑦用MnO2与浓盐酸反应制Cl2
II.某校化学研究性学习小组对浓硫酸与金属锌的反应进行探究.首先按图2组装好实验装置,然后取一定量的浓硫酸与足量Zn充分反应,微热试管A,实验过程中先观察到C、D中均有气泡产生,D中开始出现浑浊,后浑浊消失,随后气泡量逐渐减少,品红溶液褪色,反应较长时间后,C、D中的气泡量又会明显增加.
试回答:
(1)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接
3或4
3或4
、4或3
4或3
接b,c接1
1
、2
2
接d;(2)D、E试管中CCl4溶液的作用是防止溶液倒吸,该实验中起到同样作用的装置是
乙
乙
;(3)能证明浓硫酸具有强氧化性的实验现象为
C中品红溶液褪色
C中品红溶液褪色
;(4)反应较长时间后气泡量又会明显增加的原因是
浓H2SO4变成稀H2SO4,与Zn反应放出H2
浓H2SO4变成稀H2SO4,与Zn反应放出H2
;(5)D中浑浊消失的离子方程式为
SO2+CaSO3+H2O=Ca2++2HSO3-
SO2+CaSO3+H2O=Ca2++2HSO3-
.