摘要:C2H6+3.5O2→2CO2+3H2O通过分析找出一般规律.设烃CxHy为1moly=4.总体积不变.△V=0y<4.总体积减小.△V=1-y/4y>4.总体积增大.△V=y/4-1[评价]评价学生的分析.指出如果温度低于100℃生成液态水.则不符合此规律.具体情况可通过化学方程式分析.[练习]
网址:http://m.1010jiajiao.com/timu_id_237636[举报]
(2012?杭州一模)(1)当乙烯气体在空气中的体积分数为16%时遇明火会发生猛烈爆炸,若爆炸时乙烯和氧气都几乎耗尽,爆炸时发生的主要反应的化学方程式是
A.C2H4+3O2→2CO2+2H2O
B.C2H4+O2→2C+2H2O
C.C2H4+2O2→2CO+2H2O
D.2C2H4+5O2→2CO2+2CO+4H2O
E.2C2H4+3O2→2C+2CO+4H2O
(2)为测定漂白粉有效成分的质量分数,称取2.000g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol?L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3ClO-+I-═3Cl-+IO3-; IO3-+5I-+3H2O═6OH-+3l2
实验测得数据如下表所示:
该漂白粉中有效成分的质量分数为
查看习题详情和答案>>
B
B
.A.C2H4+3O2→2CO2+2H2O
B.C2H4+O2→2C+2H2O
C.C2H4+2O2→2CO+2H2O
D.2C2H4+5O2→2CO2+2CO+4H2O
E.2C2H4+3O2→2C+2CO+4H2O
(2)为测定漂白粉有效成分的质量分数,称取2.000g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol?L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3ClO-+I-═3Cl-+IO3-; IO3-+5I-+3H2O═6OH-+3l2
实验测得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
21.45%
21.45%
.(1)当乙烯气体在空气中的体积分数为16%时遇明火会发生猛烈爆炸,若爆炸时乙烯和氧气都几乎耗尽,爆炸时发生的主要反应的化学方程式是______.
A.C2H4+3O2→2CO2+2H2O
B.C2H4+O2→2C+2H2O
C.C2H4+2O2→2CO+2H2O
D.2C2H4+5O2→2CO2+2CO+4H2O
E.2C2H4+3O2→2C+2CO+4H2O
(2)为测定漂白粉有效成分的质量分数,称取2.000g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol?L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3ClO-+I-═3Cl-+IO3-; IO3-+5I-+3H2O═6OH-+3l2
实验测得数据如下表所示:
该漂白粉中有效成分的质量分数为______.
查看习题详情和答案>>
A.C2H4+3O2→2CO2+2H2O
B.C2H4+O2→2C+2H2O
C.C2H4+2O2→2CO+2H2O
D.2C2H4+5O2→2CO2+2CO+4H2O
E.2C2H4+3O2→2C+2CO+4H2O
(2)为测定漂白粉有效成分的质量分数,称取2.000g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol?L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3ClO-+I-═3Cl-+IO3-; IO3-+5I-+3H2O═6OH-+3l2
实验测得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
 (1)A.碳酸氢钠 B.阿斯匹林 C.苯甲酸钠D.柠檬黄 E.青霉素
(1)A.碳酸氢钠 B.阿斯匹林 C.苯甲酸钠D.柠檬黄 E.青霉素请用字母填空:
具有解热镇痛疗效的是
B
B
,可用作食品防腐剂的是C
C
,常用作食品着色剂的是D
D
,常用作治疗胃酸过多的抗酸剂的是A
A
.具有杀菌消炎作用的是E
E
.(2)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证.
①维生素C能增强人体对疾病的抵抗能力,促进人体生长发育,中学生每天要补充60mg的维生素C.下列物质含有丰富维生素C的是
B
B
(填字母).A.牛肉 B.辣椒 C.鸡蛋
②青少年及成人缺乏某种微量元素将导致甲状腺肿大,而且会造成智力损害,该微量元素是
A
A
(填字母) A.碘 B.铁 C.钙
③蛋白质是人体必需的营养物质,它在人体内最终分解为
B
B
(填字母).A.葡萄糖 B.氨基酸 C.脂肪酸
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处.
①汽车尾气需要用催化转化器减少有毒气体排放.写出汽车尾气中CO、NO相互作用生成可参与大气循环的两种气体的化学方程式
2NO+2CO
N2+2CO2
| ||
2NO+2CO
N2+2CO2
| ||
②对垃圾需要分类处理.如图所示的垃圾分类标志的含义是
可循环利用的物质
可循环利用的物质
.③pH<
5.6
5.6
的雨水称为酸雨;向煤中加入适量的石灰石或者生石灰
石灰石或者生石灰
,可以大大减少燃物产物中SO2的量. 天然水中杂质较多,常需加入明矾、ClO2等物质处理后才能饮用.加入ClO2的作用是杀菌消毒
杀菌消毒
;加入明矾后,Al3+水解的离子方程式是Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.有人设计了一种乙醇燃料电池,一个电极通入空气,另一个电极通入乙醇蒸汽.电池的固定电解质是晶格掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-离子.
(1)该电极负极发生的反应是
(2)乙醇的制备可以用CO2和氢气为原料,在催化剂作用下发生如下反应,
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
①写出反应的平衡常数表达式K=
.
②1m3(标准状况)CO2按上式完全反应,产生CH3CH2OH
③在一定压强下,n(H2)/n(CO2)=2,测得反应的实验数据如下表:
根据表中数据分析:
ⅰ.该反应是
ⅱ.提高
的值,K值
ⅲ.如图是某条件下H2的浓度随时间的变化曲线,若增大压强,其他条件不变,请在原图中画出H2的浓度随时间的变化曲线.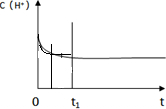

(3)有人认为乙醇的来源成本比较高,为降低成本,可以设计汽油燃料电池,但却存在一个最大问题,你认为该问题是
查看习题详情和答案>>
(1)该电极负极发生的反应是
C2H5OH-12e-=2CO2+3H2O
C2H5OH-12e-=2CO2+3H2O
.固体电解质中的O2-向负
负
极方向移动.(2)乙醇的制备可以用CO2和氢气为原料,在催化剂作用下发生如下反应,
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011①写出反应的平衡常数表达式K=
| c(CH3CH2OH)×c3(H2O) |
| c2(CO2)×c6(H2) |
| c(CH3CH2OH)×c3(H2O) |
| c2(CO2)×c6(H2) |
②1m3(标准状况)CO2按上式完全反应,产生CH3CH2OH
22.3
22.3
mol.③在一定压强下,n(H2)/n(CO2)=2,测得反应的实验数据如下表:
| 温度(K) | 500 | 600 | 700 | 800 |
| CO2转化率(%) | 60 | 43 | 28 | 15 |

ⅰ.该反应是
放热
放热
反应(填“放热”或“吸热”),升高温度,平衡常数K值减小
减小
(填“增大”、“减小”或“不变”).ⅱ.提高
| n(H2) |
| n(CO2) |
不变
不变
(填“增大”、“减小”或“不变”),对生产乙醇有利
有利
(填“有利”或“不利”).ⅲ.如图是某条件下H2的浓度随时间的变化曲线,若增大压强,其他条件不变,请在原图中画出H2的浓度随时间的变化曲线.


(3)有人认为乙醇的来源成本比较高,为降低成本,可以设计汽油燃料电池,但却存在一个最大问题,你认为该问题是
电极的气体管道溶液被堵塞
电极的气体管道溶液被堵塞
.造成这种问题的主要原因是汽油不完全燃烧产生碳黑
汽油不完全燃烧产生碳黑
.写出下列反应化学方程式或离子方程式
(1)过氧化钠可用在呼吸面具里作为氧气的来源,其反应的化学方程式为
(2)氢氧化铝可用作治疗胃酸过多的药剂,其原理用离子方程式表示为
(3)氢氧化亚铁被氧气氧化的化学方程式
(4)“雷雨发庄稼”有哪些科学道理,试解释原因(用有关反应的化学方程式表示):
(5)实验室制氨气的化学方程式:
(6)铜与浓硝酸反应的离子方程式:
查看习题详情和答案>>
(1)过氧化钠可用在呼吸面具里作为氧气的来源,其反应的化学方程式为
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
;(2)氢氧化铝可用作治疗胃酸过多的药剂,其原理用离子方程式表示为
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
;(3)氢氧化亚铁被氧气氧化的化学方程式
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
;(4)“雷雨发庄稼”有哪些科学道理,试解释原因(用有关反应的化学方程式表示):
N2+O2
2NO、2NO+O2═2NO2 、3NO2+H2O═2HNO3+NO
| ||
N2+O2
2NO、2NO+O2═2NO2 、3NO2+H2O═2HNO3+NO
;
| ||
(5)实验室制氨气的化学方程式:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
;
| ||
(6)铜与浓硝酸反应的离子方程式:
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
.