题目内容
有人设计了一种乙醇燃料电池,一个电极通入空气,另一个电极通入乙醇蒸汽.电池的固定电解质是晶格掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-离子.
(1)该电极负极发生的反应是
(2)乙醇的制备可以用CO2和氢气为原料,在催化剂作用下发生如下反应,
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
①写出反应的平衡常数表达式K=
.
②1m3(标准状况)CO2按上式完全反应,产生CH3CH2OH
③在一定压强下,n(H2)/n(CO2)=2,测得反应的实验数据如下表:
根据表中数据分析: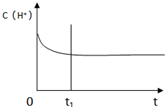
ⅰ.该反应是
ⅱ.提高
的值,K值
ⅲ.如图是某条件下H2的浓度随时间的变化曲线,若增大压强,其他条件不变,请在原图中画出H2的浓度随时间的变化曲线.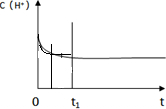

(3)有人认为乙醇的来源成本比较高,为降低成本,可以设计汽油燃料电池,但却存在一个最大问题,你认为该问题是
(1)该电极负极发生的反应是
C2H5OH-12e-=2CO2+3H2O
C2H5OH-12e-=2CO2+3H2O
.固体电解质中的O2-向负
负
极方向移动.(2)乙醇的制备可以用CO2和氢气为原料,在催化剂作用下发生如下反应,
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011①写出反应的平衡常数表达式K=
| c(CH3CH2OH)×c3(H2O) |
| c2(CO2)×c6(H2) |
| c(CH3CH2OH)×c3(H2O) |
| c2(CO2)×c6(H2) |
②1m3(标准状况)CO2按上式完全反应,产生CH3CH2OH
22.3
22.3
mol.③在一定压强下,n(H2)/n(CO2)=2,测得反应的实验数据如下表:
| 温度(K) | 500 | 600 | 700 | 800 |
| CO2转化率(%) | 60 | 43 | 28 | 15 |

ⅰ.该反应是
放热
放热
反应(填“放热”或“吸热”),升高温度,平衡常数K值减小
减小
(填“增大”、“减小”或“不变”).ⅱ.提高
| n(H2) |
| n(CO2) |
不变
不变
(填“增大”、“减小”或“不变”),对生产乙醇有利
有利
(填“有利”或“不利”).ⅲ.如图是某条件下H2的浓度随时间的变化曲线,若增大压强,其他条件不变,请在原图中画出H2的浓度随时间的变化曲线.


(3)有人认为乙醇的来源成本比较高,为降低成本,可以设计汽油燃料电池,但却存在一个最大问题,你认为该问题是
电极的气体管道溶液被堵塞
电极的气体管道溶液被堵塞
.造成这种问题的主要原因是汽油不完全燃烧产生碳黑
汽油不完全燃烧产生碳黑
.分析:(1)乙醇燃料电池负极发生氧化反应,电池工作时,阴离子向负极移动,阳离子向正极移动,注意电解质离子的种类;
(2)①根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积列平衡常数的表达式;
②根据化学方程式进行计算;
③由表中数据可知温度升高CO2转化率减小,说明升高温度平衡向逆反应方向移动,正反应放热,则有:
ⅰ、升高温度平衡向逆反应方向移动,K减小;
ⅱ、K只与温度有关,提高
的值有利于平衡向正反应方向移动;
ⅲ、增大压强,反应速率加大,平衡向正反应方向移动,达新平衡后,氢气的浓度大于原平衡浓度;
(3)如空气的量不足,会导致汽油不完全燃烧产生炭黑而导致气体管道被堵塞;
(2)①根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积列平衡常数的表达式;
②根据化学方程式进行计算;
③由表中数据可知温度升高CO2转化率减小,说明升高温度平衡向逆反应方向移动,正反应放热,则有:
ⅰ、升高温度平衡向逆反应方向移动,K减小;
ⅱ、K只与温度有关,提高
| n(H2) |
| n(CO2) |
ⅲ、增大压强,反应速率加大,平衡向正反应方向移动,达新平衡后,氢气的浓度大于原平衡浓度;
(3)如空气的量不足,会导致汽油不完全燃烧产生炭黑而导致气体管道被堵塞;
解答:解:(1)乙醇燃料电池负极发生氧化反应,电极负极发生的反应是C2H5OH-12e-+6O2-=2CO2+3H2O,电池工作时,阴离子向负极移动,阳离子向正极移动,
故答案为:C2H5OH-12e-+6O2-=2CO2+3H2O;负;
(2)①平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,K=
,
故答案为:
;
②根据化学方程式计算,1m3(标准状况)CO2的物质的量为
=44.6mol,
产生CH3CH2OH 的物质的量为
×44.6mol=22.3mol,
故答案为:22.3;
③ⅰ、由表中数据可知温度升高CO2转化率减小,说明升高温度平衡向逆反应方向移动,正反应放热,K减小,
故答案为:放热;减小;
ⅱ、K只与温度有关,提高
的值有利于平衡向正反应方向移动,故答案为:不变;有利;
ⅲ、增大压强,反应速率加大,平衡向正反应方向移动,达新平衡后,氢气的浓度大于原平衡浓度
故答案为: ;
;
(3)如使用汽油,如空气的量不足,会导致汽油不完全燃烧产生炭黑而导致气体管道被堵塞,
故答案为:电极的气体管道溶液被堵塞;汽油不完全燃烧产生碳黑.
故答案为:C2H5OH-12e-+6O2-=2CO2+3H2O;负;
(2)①平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,K=
| c(CH3CH2OH)×c3(H2O) |
| c2(CO2)× c6(H2) |
故答案为:
| c(CH3CH2OH)×c3(H2O) |
| c2(CO2)× c6(H2) |
②根据化学方程式计算,1m3(标准状况)CO2的物质的量为
| 1000L |
| 22.4L/mol |
产生CH3CH2OH 的物质的量为
| 1 |
| 2 |
故答案为:22.3;
③ⅰ、由表中数据可知温度升高CO2转化率减小,说明升高温度平衡向逆反应方向移动,正反应放热,K减小,
故答案为:放热;减小;
ⅱ、K只与温度有关,提高
| n(H2) |
| n(CO2) |
ⅲ、增大压强,反应速率加大,平衡向正反应方向移动,达新平衡后,氢气的浓度大于原平衡浓度
故答案为:
 ;
;(3)如使用汽油,如空气的量不足,会导致汽油不完全燃烧产生炭黑而导致气体管道被堵塞,
故答案为:电极的气体管道溶液被堵塞;汽油不完全燃烧产生碳黑.
点评:本题考查较为综合,题目难度较大,本题易错点为电极方程式的书写,注意把握原电池正负极的反应,利用守恒的方法进行书写.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
有人设计了一种乙醇燃料电池,一个电极通入空气,另一个电极通入乙醇蒸汽.电池的固定电解质是晶格掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-离子.
(1)该电极负极发生的反应是______.固体电解质中的O2-向______极方向移动.
(2)乙醇的制备可以用CO2和氢气为原料,在催化剂作用下发生如下反应,
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
①写出反应的平衡常数表达式K=______.
②1m3(标准状况)CO2按上式完全反应,产生CH3CH2OH______mol.
③在一定压强下,n(H2)/n(CO2)=2,测得反应的实验数据如下表:
根据表中数据分析:
ⅰ.该反应是______反应(填“放热”或“吸热”),升高温度,平衡常数K值______(填“增大”、“减小”或“不变”).
ⅱ.提高 的值,K值______(填“增大”、“减小”或“不变”),对生产乙醇______(填“有利”或“不利”).
的值,K值______(填“增大”、“减小”或“不变”),对生产乙醇______(填“有利”或“不利”).
ⅲ.如图是某条件下H2的浓度随时间的变化曲线,若增大压强,其他条件不变,请在原图中画出H2的浓度随时间的变化曲线.______
(3)有人认为乙醇的来源成本比较高,为降低成本,可以设计汽油燃料电池,但却存在一个最大问题,你认为该问题是______.造成这种问题的主要原因是______.

(1)该电极负极发生的反应是______.固体电解质中的O2-向______极方向移动.
(2)乙醇的制备可以用CO2和氢气为原料,在催化剂作用下发生如下反应,
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011①写出反应的平衡常数表达式K=______.
②1m3(标准状况)CO2按上式完全反应,产生CH3CH2OH______mol.
③在一定压强下,n(H2)/n(CO2)=2,测得反应的实验数据如下表:
| 温度(K) | 500 | 600 | 700 | 800 |
| CO2转化率(%) | 60 | 43 | 28 | 15 |
ⅰ.该反应是______反应(填“放热”或“吸热”),升高温度,平衡常数K值______(填“增大”、“减小”或“不变”).
ⅱ.提高
 的值,K值______(填“增大”、“减小”或“不变”),对生产乙醇______(填“有利”或“不利”).
的值,K值______(填“增大”、“减小”或“不变”),对生产乙醇______(填“有利”或“不利”).ⅲ.如图是某条件下H2的浓度随时间的变化曲线,若增大压强,其他条件不变,请在原图中画出H2的浓度随时间的变化曲线.______
(3)有人认为乙醇的来源成本比较高,为降低成本,可以设计汽油燃料电池,但却存在一个最大问题,你认为该问题是______.造成这种问题的主要原因是______.

 Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.
Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.