网址:http://m.1010jiajiao.com/timu_id_235784[举报]
1.B 2.D 3.B 4.D 5.A 6.C 7.AB 8.C 9.A 10.AD 11.CD
12.B 13.C 14.C 15.C 16.C 17.D 18.C 19.D 20.C 21.D 22.B
23.本题考查学生称量、加热、溶解、结晶等基本操作,同时要求理论联系实际确定有关化学方程式和计算溶解度.
通过计算知:用50 mL
70℃热水与24 gKCl制几乎饱和的溶液,再用25 mL 70℃热水与 配制成饱和溶液,将此两种溶液混合、搅匀、静止、冷却,将陆续析出
配制成饱和溶液,将此两种溶液混合、搅匀、静止、冷却,将陆续析出 晶体,至20℃时,减压过滤使
晶体,至20℃时,减压过滤使 分离出来.
分离出来.
24.(1)无机酸酯

(2)X可能是沸石(或碎瓷片);防止暴沸
(3)回流冷凝易挥发的反应物:a;b
(4)用足量水洗涤,分液除去乙醇,加稀NaOH溶液,分液除去碘.
25.(1)C→B→D→A→G→H→E→F
(2)使漏斗下端管口紧靠烧杯内壁;及时关闭活塞,不要让上层液体流出;使漏斗内外空气相通以保证(G)操作时漏斗里液体能够流出.
(3) 与水不互溶;而且碘在
与水不互溶;而且碘在 中的溶解度比在水中大很多.
中的溶解度比在水中大很多.
(4)A、C
提示:(4)热裂汽油中含有不饱和气态烃如丙烯、丁烯与溴发生加成反应.
26.(1)AEF (2)AB (3)AF(或AEF) (4)D (5)安全瓶防止碱液倒吸
27.(1)4 a、d、f、h h吸收 吸收
吸收 天平
天平
(2)试样质量=碳元素质量+氢元素质量为烃
试样质量>碳元素质量+氢元素质量为烃的含氧衍生物
(3)B
28.(1)
(2)碱石灰;无水 只能吸水,不能吸收
只能吸水,不能吸收 .
.
(3) (或
(或 )
)
(4) ;放热;反应开始后断开电键K,铂丝能继续保持红热.
;放热;反应开始后断开电键K,铂丝能继续保持红热.
(5)气体颜色变浅; 发生反应:
发生反应:

 ,属于放热反应,达到平衡后,若降低温度,平衡向右移动,
,属于放热反应,达到平衡后,若降低温度,平衡向右移动, 浓度减少,
浓度减少, 浓度增大,而
浓度增大,而 无色,所以气体颜色变浅.
无色,所以气体颜色变浅.
29.本题考查学生乙炔的制取方法、干燥、氧化原理及产物的吸收测定顺序.由于制得的乙炔气含水对燃烧及产物测定有影响,故制得的乙炔气体必须先干燥,然后再进行题中的催化氧化,乃至测定产物的质量.所以(1)G、E、F、H、I、C、D、A
(2)吸收燃烧产生的 气体;吸收产生的水蒸气;吸收乙炔中的水蒸气.
气体;吸收产生的水蒸气;吸收乙炔中的水蒸气.
(3)

(4)
30.解析:过程如下:


答案:①将废水过滤,目的是除去其中的悬浮泥沙等不溶物;
②往①的滤液中加入足量锌粉,将其中的 置换出来;
置换出来;
③过滤②中的不溶物,滤出Ag和过量的锌粉;
④往③的滤渣中加入过量的稀硫酸,使其中的锌粉转化为 而进入溶液;
而进入溶液;
⑤过滤,将④中没溶解的Ag滤出回收;
⑥将③、⑤得到的滤液合并,蒸发浓缩,使 析出后回收.
析出后回收.
| 物质 | Al | A12O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1565 |
| 沸点/℃ | 2467 | 2980 | 2750 | ---- |
(1)铝热反应是氧化还原反应,在反应中金属铝表现出
(2)某同学根据以上数据推测,铝热反应所得到的熔融物中应含有铁、铝两种金属.如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为
(3)另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3.则
①物质甲是
②该同学的实验方案是否合理?答:
(4)把l5.12g Fe、Fe2O3和Al的混合物与0.5L 2mol?L-1稀硫酸(足量)充分反应,生成氢气n mol.则
①用浓硫酸配制0.5L 2mol?L-1的稀硫酸需要的玻璃仪器有烧杯、500mL容量瓶、量筒和
②n的取值范围是
③向反应后的混合溶液中滴加NaOH溶液,当产生沉淀的量达到最大时,参加反应的NaOH的物质的量为
 (2010?广东)硼酸(H3BO3)在食品、医药领域应用广泛.
(2010?广东)硼酸(H3BO3)在食品、医药领域应用广泛.(1)请完成B2H6气体与水反应的化学方程式:B2H6+6H2O=2H3BO3+
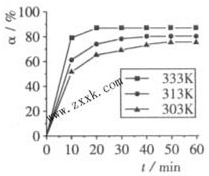
(2)在其他条件相同时,反应H3BO3+3CH3OH
 B(OCH3)3+3H2O中,H3BO3的转化率(a)在不同温度下随反应时间(t)的变化见图,由此图可得出:
B(OCH3)3+3H2O中,H3BO3的转化率(a)在不同温度下随反应时间(t)的变化见图,由此图可得出:①温度对应该反应的反应速率和平衡移动的影响是
②该反应的△H
(3)H3BO3溶液中存在如下反应:H3BO3(aq)+H2O(l)
 [B(OH)4]-( aq)+H+(aq)已知0.70mol?L-1 H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0×10-5mol?L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
[B(OH)4]-( aq)+H+(aq)已知0.70mol?L-1 H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0×10-5mol?L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)| 物质 | Al | A12O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1565 |
| 沸点/℃ | 2467 | 2980 | 2750 | ---- |
(1)铝热反应是氧化还原反应,在反应中金属铝表现出______性 (填“氧化”或“还原”).
(2)某同学根据以上数据推测,铝热反应所得到的熔融物中应含有铁、铝两种金属.如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为______,可观察到的实验现象是______.
(3)另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3.则
①物质甲是______ (填化学式).
②该同学的实验方案是否合理?答:______ (填“合理”或“不合理”).
(4)把l5.12g Fe、Fe2O3和Al的混合物与0.5L 2mol-L-1稀硫酸(足量)充分反应,生成氢气n mol.则
①用浓硫酸配制0.5L 2mo1-L-1的稀硫酸需要的玻璃仪器有烧杯、500mL容量瓶、量筒和______、______.
②n的取值范围是______.
③向反应后的混合溶液中滴加NaOH溶液,当产生沉淀的量达到最大时,参加反应的NaOH的物质的量为______ mol.

图3-2
(1)电池中的质子交换膜只允许质子和水分子通过。电池工作时,质子移向电源的___________极,铂碳上所发生的电极反应式为_________________________________________________。
(2)葡萄糖的燃烧热为2800kJ/mol,写出葡萄糖燃烧的热化学方程式:__________________。
(3)化学需氧量(COD)是重要的水质指标,其数值表示将
序号 | A | B | C | D | E |
污水类型 | 生活污水 | 印染 | 电镀 | 造纸 | 硫酸工业废水 |
COD值/(mg/L) | 520 | 870 | 20 | 960 | 120 |
(4)在化学工作者的眼中,“垃圾是放错了位置的资源”。写出硫酸工业“废气”处理利用的化学方程式:____________________________________________。
查看习题详情和答案>>| 物质 | Al | A12O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1565 |
| 沸点/℃ | 2467 | 2980 | 2750 | ---- |
(1)铝热反应是氧化还原反应,在反应中金属铝表现出______性 (填“氧化”或“还原”).
(2)某同学根据以上数据推测,铝热反应所得到的熔融物中应含有铁、铝两种金属.如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为______,可观察到的实验现象是______.
(3)另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3.则
①物质甲是______ (填化学式).
②该同学的实验方案是否合理?答:______ (填“合理”或“不合理”).
(4)把l5.12g Fe、Fe2O3和Al的混合物与0.5L 2mol?L-1稀硫酸(足量)充分反应,生成氢气n mol.则
①用浓硫酸配制0.5L 2mo1?L-1的稀硫酸需要的玻璃仪器有烧杯、500mL容量瓶、量筒和______、______.
②n的取值范围是______.
③向反应后的混合溶液中滴加NaOH溶液,当产生沉淀的量达到最大时,参加反应的NaOH的物质的量为______ mol.
查看习题详情和答案>>