摘要:c[评价]
网址:http://m.1010jiajiao.com/timu_id_234202[举报]
粗铜中含有少量的锌、铁、银、金等金属.某化学兴趣小组以硫酸铜溶液为电解液电解精炼钢之后,将电解液过滤得到滤液A和阳极泥,为测定滤液A中Fe2+、Cu2+的浓度,实验流程如下:
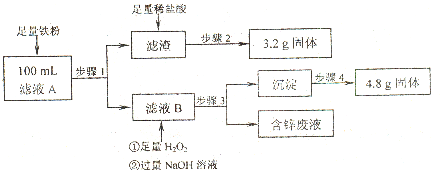
已知向c(Zn2+)=1mol/L的溶液中加入NaOH溶液,Zn(OH)2沉淀生成与溶解的pH如下:

试回答下列问题:
(1)步骤2中涉及的操作是
(2)写出Zn(OH)2的电离方程式
(3)滤液A中c(Cu2+)=
查看习题详情和答案>>

已知向c(Zn2+)=1mol/L的溶液中加入NaOH溶液,Zn(OH)2沉淀生成与溶解的pH如下:

试回答下列问题:
(1)步骤2中涉及的操作是
过滤
过滤
、洗涤、晾干、称量;步骤4中的操作次为洗涤、灼烧、冷却、称量,其中检验沉淀已经洗涤干净的方法(操作方法、现象和结论)是取少量最后一次洗涤液,滴加氯化钡溶液,若无沉淀生成,证明洗涤干净
取少量最后一次洗涤液,滴加氯化钡溶液,若无沉淀生成,证明洗涤干净
.(2)写出Zn(OH)2的电离方程式
H++HZnO2-?Zn(OH)2?Zn2++2OH2-,
H++HZnO2-?Zn(OH)2?Zn2++2OH2-,
.(3)滤液A中c(Cu2+)=
0.5
0.5
mol?L-1,c(Fe2+)=0.1
0.1
mol?L-1.中学化学中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡4种,且均符合平衡移动原理.请回答下列问题:
Ⅰ.常温下有浓度均为0.1mol?L-1的四种溶液:①NaHCO3、②Na2CO3、③HCl、④NH3?H2O.
(1)溶液①、②、③pH值由小到大的顺序为
(2)向④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值
(3)取10mL溶液③,加水稀释到100mL,则此时溶液中由水电离出的c(H+)=
(4)上述溶液中,既能与氢氧化钠溶液反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为
(5)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积
Ⅱ.难溶电解质在水溶液中存在溶解平衡.在常温下,溶液中各离子浓度以它们化学计量数为指数的乘积是一个常数,叫溶度积常数(Ksp).当溶液中各离子浓度指数的乘积大于溶度积时,则产生沉淀,反之固体溶解.若某CuSO4溶液中c(Cu2+)=0.02mol?L-1,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于
查看习题详情和答案>>
Ⅰ.常温下有浓度均为0.1mol?L-1的四种溶液:①NaHCO3、②Na2CO3、③HCl、④NH3?H2O.
(1)溶液①、②、③pH值由小到大的顺序为
③<①<②
③<①<②
.(填序号)(2)向④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值
增大
增大
(填“增大”、“减小”或“不变”).(3)取10mL溶液③,加水稀释到100mL,则此时溶液中由水电离出的c(H+)=
10-12 mol?L-1
10-12 mol?L-1
.(4)上述溶液中,既能与氢氧化钠溶液反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为
c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-)
c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-)
.(5)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积
小于
小于
④的体积(填“大于”、“小于”或“等于”).Ⅱ.难溶电解质在水溶液中存在溶解平衡.在常温下,溶液中各离子浓度以它们化学计量数为指数的乘积是一个常数,叫溶度积常数(Ksp).当溶液中各离子浓度指数的乘积大于溶度积时,则产生沉淀,反之固体溶解.若某CuSO4溶液中c(Cu2+)=0.02mol?L-1,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于
5
5
(已知Ksp=2.0×10-20).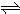 Cu2++2OH-,Ksp=c(Cu2+)?[c(OH-)]2=2×10-20.当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
Cu2++2OH-,Ksp=c(Cu2+)?[c(OH-)]2=2×10-20.当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.