题目内容
(1)某CuSO4溶液里c(Cu2+)=0.02mol?L-1,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于
(2)要使0.2mol?L-1 CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为
(2)Cu2+沉淀较为完全浓度降至原来的千分之一,根据Ksp求出OH-离子的浓度,再求pH.
|
| 1×10-14 |
| 10-9 |
所以pH≥-lg(10-5)=5,故答案为:5;
(2)Cu2+沉淀较为完全是的浓度为
| 0.2mol/L |
| 1000 |
则c(OH-)=
|
则c(H+)=
| 1×10-14 |
| 10-8 |
所以pH=-lg(10-6)=6,
故答案为:6.

(14分)某科研小组探究工业废Cu粉(杂质含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4·5H2O,实现废物综合利用,实验过程如下:
Ⅰ: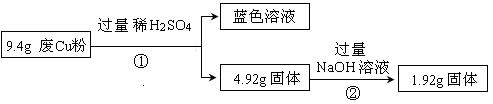
(1) 废Cu粉中一定含有的杂质是 。
(2) 分别写出过程①、②发生反应的离子方程式:
① ;
② 。
Ⅱ: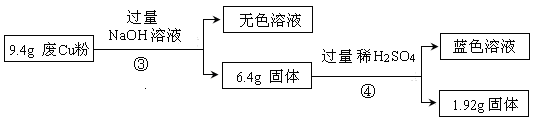
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是 (不必化简)。
Ⅲ:已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积(Ksp) | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
(5)下列与Ⅲ方案相关的叙述中,正确的是 (填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH选择的试剂可以是氢氧化铜或氧化铜
D.在pH>4的溶液中Fe3+一定不能大量存在
(15分)制取纯净的氯化铜晶体(CuCl2·2H2O)的生产过程如下:
I.将粗氧化铜(含少量Fe)溶解在足量的稀盐酸中,然后加热、过滤得到CuCl2(含少量FeCl2)溶液,经测定,溶液pH为2。
II.对I中所得到的溶液按下列步骤进行提纯。
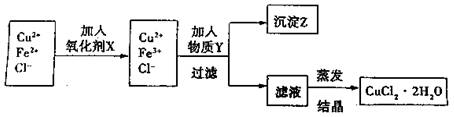
已知:
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ |
1.9 |
3.2 |
|
Cu2+ |
4.7 |
6.7 |
试回答下列问题:
(1)下列物质中,最适合作为氧化剂X的是 。(填序号)
A.KMnO4 B.K2Cr2O4 C.H2O2 D.NaClO
(2)①加紧入的物质Y是 。
②写出沉淀Z在水中的沉淀溶解平衡方程式: 。
(3)分离出沉淀Z,并将滤液蒸发,欲获得氯化铜晶体(CuCl2·2H2O),应采取的措施是 。
(4)①某同学利用反应:Cu+2H+===Cu2++H2↑设计实验来制取CuCl2溶液,该同学设计的装置应该为 。(填“原电池”或“电解池”)
②请你在下面方框中画出该同学设计的装置图,并指明电极材料和电解质溶液。

(5)已知一些难溶物的浓度积常数如下表:
|
物质 |
FeS |
MnS |
CuS |
PbS |
HgS |
ZnS |
|
Ksp |
6.3×10-18 |
2.5×-13 |
1.3×10-36 |
3.4×10-28 |
6.4×10-53 |
1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的 除去它们。(选填序号)
①NaOH ②FeS ③Na2S

 Fe2+(aq)+3OH-(aq)
Fe2+(aq)+3OH-(aq)