摘要:写出C5H12.C4H8分别属于烷烃和烯烃的同分异构体
网址:http://m.1010jiajiao.com/timu_id_220928[举报]
利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.请回答下列问题:
(1)已知COCl2分子的结构式为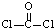 ,则COCl2分子内含有
,则COCl2分子内含有
A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3 个σ键、1个π键
(2)Fe(CO)5中铁的化合价为0,写出Fe元素基态原子的价电子排布式
Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可以判断Fe(CO)5晶体类型为
(3)Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是
(4)与CO分子互为等电子体的分子和离子各写出1种,分别为
查看习题详情和答案>>
(1)已知COCl2分子的结构式为
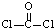 ,则COCl2分子内含有
,则COCl2分子内含有D
D
(填标号);A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3 个σ键、1个π键
(2)Fe(CO)5中铁的化合价为0,写出Fe元素基态原子的价电子排布式
3d64s2
3d64s2
;Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可以判断Fe(CO)5晶体类型为
分子晶体
分子晶体
.(3)Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是
金属键
金属键
.(4)与CO分子互为等电子体的分子和离子各写出1种,分别为
N2
N2
和CN-
CN-
(填化学式).(1)下表为原子序数依次增大的短周期元素A~ E的第一到第五电离能数据.
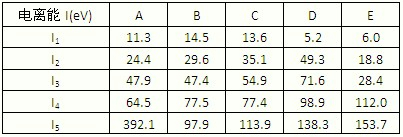
请回答:表中的金属元素是
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,石墨烯的碳源可以由一氧化碳、乙醇、酞菁等中的一种或任意组合提供.
①钴原子在基态时,核外电子排布式为
②乙醇沸点比氯乙烷高,主要原因是
③与CO分子互为等电子体的分子和离子各写出1种,分别为
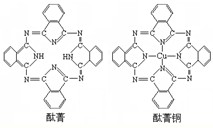
④酞菁与酞菁铜染料分子结构如图,酞菁分子中氮原子采用的杂化方式是
查看习题详情和答案>>

请回答:表中的金属元素是
DE
DE
(填字母),其中化合价为+3价的是E
E
(填字母);若A、B、C依次为同周期相邻元素,表中显示B比A和C的第一电离能都略大,其原因是B的np轨道上的电子半满,能量比A和C低,第一电离能比A和C大
B的np轨道上的电子半满,能量比A和C低,第一电离能比A和C大
.(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,石墨烯的碳源可以由一氧化碳、乙醇、酞菁等中的一种或任意组合提供.
①钴原子在基态时,核外电子排布式为
[Ar]3d74s2
[Ar]3d74s2
.②乙醇沸点比氯乙烷高,主要原因是
乙醇分子间可形成氢键,而氯乙烷分子间无氢键
乙醇分子间可形成氢键,而氯乙烷分子间无氢键
.③与CO分子互为等电子体的分子和离子各写出1种,分别为
N2
N2
和CN-
CN-
(填化学式)④酞菁与酞菁铜染料分子结构如图,酞菁分子中氮原子采用的杂化方式是
sp3和sp2
sp3和sp2
;酞菁铜分子中心原子的配位数为2
2
.
 (2010?大连二模)[选修-物质结构与性质]
(2010?大连二模)[选修-物质结构与性质]羰基铁[Fe(CO)5]会使合成甲醇和合成氨等生产过程中的催化剂中素.请回答下列问题:
(1)Fe(CO)5中铁的化合价为0,写出铁原子的基态电子排布式
[Ar]3d64s2
[Ar]3d64s2
.(2)CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO分子中C原子的杂化类型为
sp
sp
杂化.与CO分子互为等电子体的分子和离子各写出1种,分别为N2
N2
和CN-
CN-
(填化学式),CO分子的结构式可表示为C≡O
C≡O
.(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可以判断Fe(CO)5晶体为
分子晶体
分子晶体
.(4)科学家通过X射线探明,FeO、MgO、CaO的晶体结构与NaCl的晶体结构相似(如图所示)①比较晶体熔点的高低MgO
高于
高于
CaO(填“高于”或“低于”)②若在FeO晶体中阴阳离子间最近距离为a cm,晶体密度为dg/cm3.则阿伏伽德罗常数NA表达式为
| 36 |
| da3 |
| 36 |
| da3 |