摘要:33.FeCl2 KCl (2)Fe+2H+=Fe2++H2↑ 2+O2+2H2O=4Fe(OH)3 Fe+2FeCl3=3FeCl2
网址:http://m.1010jiajiao.com/timu_id_213456[举报]
(1)鉴别KCl溶液和K2CO3的试剂是
(2)除去NaCO3粉末中混入的NaHCO3杂质用
(3)除去FeCl2溶液中混有的FeCl3,加入的试剂是
查看习题详情和答案>>
盐酸
盐酸
,离子方程式为CO32-+2H+═H2O+CO2↑
CO32-+2H+═H2O+CO2↑
.(2)除去NaCO3粉末中混入的NaHCO3杂质用
加热
加热
方法,化学方程式为2NaHCO3
Na2CO3+H2O+CO2↑
| ||
2NaHCO3
Na2CO3+H2O+CO2↑
.
| ||
(3)除去FeCl2溶液中混有的FeCl3,加入的试剂是
Fe粉
Fe粉
,离子方程式为2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.
某酸性腐蚀液中含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费.以废腐蚀液为原料,回收铜并将铁的化合物全部转化为FeCl3溶液.
测得某酸性废腐蚀液中含CuCl2 1.5mol/L,FeCl2 3mol/L,FeCl3 1mol/L,HCl 1mol/L.
取该酸性废腐蚀液200mL,按如下流程在实验室进行实验:
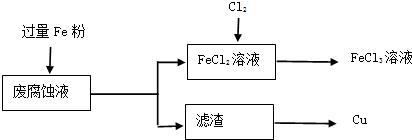
(1)腐蚀液中加入过量Fe粉,发生反应的离子方程式为 .
(2)检验废腐蚀液中含有Fe3+的实验操作是取少量废腐蚀液于试管中,滴加几滴KSCN溶液,溶液 ,则证明原溶液中含有Fe3+.
(3)滤渣的主要成分是 (填化学式).由滤渣得到铜除杂所需试剂是 .
(4)FeCl2溶液中通入Cl2,发生反应的化学方程式为 .
(5)实验室用固体KClO3与浓HCl反应制Cl2,反应的化学方程式为:KClO3+6HCl(浓)═KCl+3Cl2+3H2O若反应生成6.72L(标准状况)Cl2,转移的电子数为 mol.
(6)按上述流程操作,加入Fe粉的质量应不少于 g.
查看习题详情和答案>>
测得某酸性废腐蚀液中含CuCl2 1.5mol/L,FeCl2 3mol/L,FeCl3 1mol/L,HCl 1mol/L.
取该酸性废腐蚀液200mL,按如下流程在实验室进行实验:

(1)腐蚀液中加入过量Fe粉,发生反应的离子方程式为
(2)检验废腐蚀液中含有Fe3+的实验操作是取少量废腐蚀液于试管中,滴加几滴KSCN溶液,溶液
(3)滤渣的主要成分是
(4)FeCl2溶液中通入Cl2,发生反应的化学方程式为
(5)实验室用固体KClO3与浓HCl反应制Cl2,反应的化学方程式为:KClO3+6HCl(浓)═KCl+3Cl2+3H2O若反应生成6.72L(标准状况)Cl2,转移的电子数为
(6)按上述流程操作,加入Fe粉的质量应不少于
(1)鉴别KCl溶液和K2CO3溶液的试剂是
(2)除去FeCl2溶液中的少量FeCl3,可加入
查看习题详情和答案>>
盐酸
盐酸
,离子方程式为CO32-+2H+=CO2↑+H2O
CO32-+2H+=CO2↑+H2O
(2)除去FeCl2溶液中的少量FeCl3,可加入
铁粉
铁粉
,离子方程式为2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
除去FeCl3溶液中的少量FeCl2,可加入氯气或氯水
氯气或氯水
,离子方程式为2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
除去FeCl2溶液中的少量CuCl2,可加入铁粉
铁粉
,离子方程式为Fe+Cu2+=Fe2++Cu
Fe+Cu2+=Fe2++Cu
.下列溶液中的氯离子数目与50 mL 1 mol·L-1的FeCl3溶液中氯离子数目相等的是( )
| A.50 mL 1.5 mol·L-1的FeCl2溶液 | B.100 mL 3 mol·L-1的NH4Cl溶液 |
| C.75 mL 3 mol·L-1的KCl溶液 | D.50 mL 2 mol·L-1的CaCl2溶液 |