摘要:(2)Ag++2NH3 [Ag(NH3)2]+欲使银氨溶液中转化出大量的Ag+.适宜的试剂是 A.NaOH B.HCl C.HNO3 D.NaHSO4
网址:http://m.1010jiajiao.com/timu_id_209343[举报]
一、选择题(共55分)(其中1―5每题2分共10分,6―20每题3分共45分)
1―5 BBCDB 6―10 DBBBA 11―15 BCBAB 16―20 CCCBD
二、填空题
21.(10分)(1)A:碳酸铵或碳酸氢铵(2分)
B:略 D:三角锥 G:红棕色(各1分)
(2)2CO2+2Na2O2=2Na2CO3+O2↑(2分)
(3)4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H=+108akJ?mol-1(3分)
(1)4HCl(浓盐酸)+MnO2===MnCl2+2H2O+Cl2↑(2分)
.files/image022.gif) |
(2)2Cl2+2H2O(气)+C====4HCl↑+CO2↑(2分)
吸收Cl2中的HCl气体,提供D处所需水蒸气。(1分)
(3)生成的HCl气体使紫石蕊溶液变红,因未反应完的Cl2与H2O作用产生的HClO的漂白作用使红色消失。(2分)
(4)B(1分)
(5)瓶中液面下降,长颈漏斗内液面上升;贮存少量Cl2(2)
23.(11分)(1)0.93<x(Mg)<1.57,2,55<x(N)<3.44。(各2分)
(2)同周期(同主族)中,x值越大,其原子半径越小;(2分)周期性。(1分)
(3)氮原子(1分)
(4)共价键(2分)
(5)第六周期IA族(1分)
24.(9分)(1)正向(1分) (2)B、D(2分)
(3)①n(D)>0.6mol(2分)②n(C)=1.8mol n(D)>0.5mol(各2分)
三、计算题(5分)
26.(1)66.7% (2)50
已知下列两个反应,前者较后者更易发生(1)NH3+H+?NH+4(2)Ag++2NH3?[Ag(NH3)2]+欲使银氨溶液中转化出大量的Ag+,适宜的试剂是( )
查看习题详情和答案>>
| A.NaOH | B.HCl | C.HNO3 | D.NaHSO4 |
已知下列两个反应,前者较后者更易发生(1)NH3+H+?NH+4(2)Ag++2NH3?[Ag(NH3)2]+欲使银氨溶液中转化出大量的Ag+,适宜的试剂是( )
A.NaOH
B.HCl
C.HNO3
D.NaHSO4
查看习题详情和答案>>
A.NaOH
B.HCl
C.HNO3
D.NaHSO4
查看习题详情和答案>>
(2012?北京)有文献记载:在强碱性条件下,加热银氨溶液可能析出银镜.某同学进行如下验证和对比实验.
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料:
a.Ag(NH3)2++2H2O?Ag++2NH3+H2O
b.AgOH不稳定,极易分解为黑色Ag2O
(1)配制银氨溶液所需的药品是
(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3,产生的现象是
②产生Ag2O的原因是
(3)该同学对产生银镜的原因提出瑕设:可能是NaOH还原Ag2O.实验及现象:向AgNO3溶液中加入
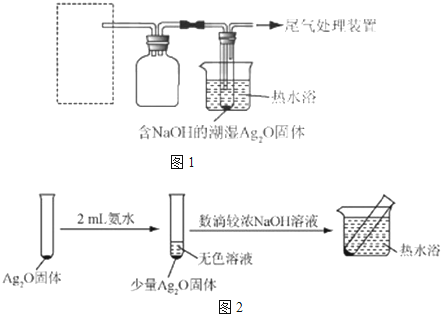
(4)重新假设:在NaOH存在下,可能是NH3还原Ag2O.用图1所示装置进行实验.现象:出现银镜.在虚线框内画出用生石灰和浓氨水制取NH3的装置简图(夹持仪器略).
(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成.由此又提出假设:在NaOH存在下,可能是Ag(NH3)2OH也参与了NH3还原Ag2O的反应.进行如图2实验:
①有部分Ag2O溶解在氨水中,该反应的化学方程式是
②实验结果证实假设成立,依据的现象是
(6)用HNO3清洗试管壁上的Ag,该反应的化学方程式是
查看习题详情和答案>>
| 装置 | 实验序号 | 试管中的药品 | 现象 |
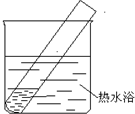 |
实验I | 2mL银氨溶液和数滴较浓NaOH溶液 | 有气泡产生; 一段时间后,溶液逐渐变黑; 试管壁附着有银镜 |
| 实验II | 2mL银氨溶液和数滴浓氨水 | 有气泡产生; 一段时间后,溶液无明显变化 |
a.Ag(NH3)2++2H2O?Ag++2NH3+H2O
b.AgOH不稳定,极易分解为黑色Ag2O
(1)配制银氨溶液所需的药品是
AgNO3溶液和浓氨水
AgNO3溶液和浓氨水
.(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3,产生的现象是
试纸变蓝
试纸变蓝
.②产生Ag2O的原因是
在NaOH存在下,加热促进NH3?H2O分解,逸出NH3,促使平衡Ag(NH3)2++2H2O?Ag++2NH3?H2O正向移动,c(Ag+)增大,Ag+与OH-反应立即转化为Ag2O:2 OH-+2 Ag+=Ag2O↓+H2O
在NaOH存在下,加热促进NH3?H2O分解,逸出NH3,促使平衡Ag(NH3)2++2H2O?Ag++2NH3?H2O正向移动,c(Ag+)增大,Ag+与OH-反应立即转化为Ag2O:2 OH-+2 Ag+=Ag2O↓+H2O
.(3)该同学对产生银镜的原因提出瑕设:可能是NaOH还原Ag2O.实验及现象:向AgNO3溶液中加入
过量NaOH溶液
过量NaOH溶液
,出现黑色沉淀;水浴加热,未出现银镜.
(4)重新假设:在NaOH存在下,可能是NH3还原Ag2O.用图1所示装置进行实验.现象:出现银镜.在虚线框内画出用生石灰和浓氨水制取NH3的装置简图(夹持仪器略).
(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成.由此又提出假设:在NaOH存在下,可能是Ag(NH3)2OH也参与了NH3还原Ag2O的反应.进行如图2实验:
①有部分Ag2O溶解在氨水中,该反应的化学方程式是
Ag2O+4 NH3?H2O=2Ag(NH3)2OH+3H2O
Ag2O+4 NH3?H2O=2Ag(NH3)2OH+3H2O
.②实验结果证实假设成立,依据的现象是
与溶液接触的试管壁上析出银镜
与溶液接触的试管壁上析出银镜
.(6)用HNO3清洗试管壁上的Ag,该反应的化学方程式是
2HNO3(浓)+Ag═Ag NO3+2NO2↑+H2O
2HNO3(浓)+Ag═Ag NO3+2NO2↑+H2O
..files/image021.gif)