摘要:26.氮氧化物(3)H2O2或PH3饱和NaHCO3溶液或Br2水或KMnO4溶液(6)次氯酸钙和氯化钙
网址:http://m.1010jiajiao.com/timu_id_195819[举报]
(2010?丰台区二模)为探究如何尽可能多的使NO2被水吸收,某活动小组设计并完成了以下实验.

(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2.
①根据反应原理他们选用了相同的装置
②写出铜与浓硝酸反应的离子方程式
③过氧化氢溶液与MnO2制取O2时,MnO2的作用是
④收集NO2可采用的收集方法是
(2)活动小组的同学做了如下准备:用气囊收集好纯净的O2;收集了一试管NO2;用干燥的烧瓶收集了一定比例的NO2和O2混合气体.
①为了尽可能多的使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通入O2相比,其优点是
②利用图4吸收气体时,其操作和现象为
③NO2、O2、H2O反应的产物为硝酸,反应中NO2和O2物质的量之比a:b=
查看习题详情和答案>>

(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2.
①根据反应原理他们选用了相同的装置
图2
图2
(填“图 1”或“图 2”)分别制取NO2 和O2.②写出铜与浓硝酸反应的离子方程式
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
.③过氧化氢溶液与MnO2制取O2时,MnO2的作用是
催化剂
催化剂
.④收集NO2可采用的收集方法是
瓶口向上排空气法
瓶口向上排空气法
.(2)活动小组的同学做了如下准备:用气囊收集好纯净的O2;收集了一试管NO2;用干燥的烧瓶收集了一定比例的NO2和O2混合气体.
①为了尽可能多的使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通入O2相比,其优点是
有利于控制氧气气流的速度(控制氧气的量)
有利于控制氧气气流的速度(控制氧气的量)
.②利用图4吸收气体时,其操作和现象为
将胶头滴管中的水挤压进烧瓶,然后打开止水夹,可以看到烧杯中的水进入烧瓶形成喷泉
将胶头滴管中的水挤压进烧瓶,然后打开止水夹,可以看到烧杯中的水进入烧瓶形成喷泉
.③NO2、O2、H2O反应的产物为硝酸,反应中NO2和O2物质的量之比a:b=
4:1
4:1
;标准状况下,若图4中混合气体NO2和O2比例为a:b,当混合气体全部被吸收时所得溶液物质的量浓度为0.036
0.036
mol/L(保留两位有效数字). 某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).
某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).(1)写出实验室制取氨气的化学方程式:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+H2O.
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+H2O.
.
| ||
(2)(每空1分)若实验室只有浓硫酸、浓盐酸、浓氨水、氢氧化钠固体、氯化铵固体、氧化钙、无水氯化钙、石蕊试液和如图1所示气体发生装置,你认为他们能制得所需的气体吗?把你的判断填入下表:
| 你的判断 | NH2 | HCl |  |
| 能够制的 | a中药品: 浓氨水 浓氨水 b中药品: 氢氧化钠固体或氧化钙 氢氧化钠固体或氧化钙 |
a中药品: 浓盐酸 浓盐酸 b中药品: 浓硫酸 浓硫酸 | |
| 不能制的 | 原因: 无 无 |
原因: 无 无 |
向上排空气
向上排空气
法,要得到干燥的氨气可选用碱石灰
碱石灰
作干燥剂.(3)如果用图2装置进行喷泉实验,上部烧瓶已装满干燥氨气,打开止水夹,挤出胶头滴管中的水引水上喷.该实验的原理是
氨气极易溶解于水,致使烧瓶内气体压强迅速减小
氨气极易溶解于水,致使烧瓶内气体压强迅速减小
.(4)如果用图3装置进行喷泉实验,上部烧瓶已装满干燥氨气气体,请说明引发喷泉的方法.
打开夹子,用手(或热毛巾)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉.
打开夹子,用手(或热毛巾)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉.
(5)若至喷泉实验停止时,图2中剩有烧瓶容积1/5的气体;图3烧瓶中剩有烧瓶容积1/4的气体;则图3烧瓶中盐酸的物质的量浓度为
| 1 |
| 22.4 |
| 1 |
| 22.4 |
等于
等于
(填“大于”、“小于”、“等于”)图3烧瓶中盐酸的物质的量浓度.(6)若使上述两种溶液混合后,溶液中铵离子和氯离子浓度相等,应如何操作:
向混合溶液中滴加氨水至溶液PH=7
向混合溶液中滴加氨水至溶液PH=7
.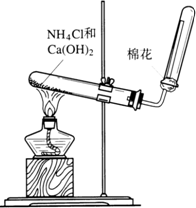 右图是实验室制取氨气的装置图.请回答:
右图是实验室制取氨气的装置图.请回答:(1)实验室制取氨气的化学方程式为
(2)因为氨气的密度比空气的
(3)干燥氨气可选用的试剂是
①碱石灰 ②浓硫酸. 查看习题详情和答案>>
(1)请针对CO2和SO2的相同点与不同点回答问题.
①它们中可以使澄清石灰水变浑浊的是 .
②它们中可以用向上排空气法收集的是 .
③它们中能使品红溶液及高锰酸钾溶液褪色的是 .
(2)现有两位同学设计了下述两个方案,并都认为如果观察到的现象和自己设计的方案一致,即可确证无色混合气体中含有CO2和SO2.
方案甲:气体通过酸性高锰酸钾溶液时溶液褪色,继续通过澄清石灰水时石灰水变浑浊.
方案乙:气体通过品红溶液时溶液红色变浅,继续通过澄清石灰水时石灰水变浑浊.
试评价上述各方案是否严密.若你认为哪个方案不严密,请简要说明理由: .
查看习题详情和答案>>
①它们中可以使澄清石灰水变浑浊的是
②它们中可以用向上排空气法收集的是
③它们中能使品红溶液及高锰酸钾溶液褪色的是
(2)现有两位同学设计了下述两个方案,并都认为如果观察到的现象和自己设计的方案一致,即可确证无色混合气体中含有CO2和SO2.
方案甲:气体通过酸性高锰酸钾溶液时溶液褪色,继续通过澄清石灰水时石灰水变浑浊.
方案乙:气体通过品红溶液时溶液红色变浅,继续通过澄清石灰水时石灰水变浑浊.
试评价上述各方案是否严密.若你认为哪个方案不严密,请简要说明理由:
实验室制取并收集氯气的装置如图1:
(1)某同学进行实验时可能有如下操作:
①连接好装置并检查气密性
②缓缓加热;
③在烧瓶里加入MnO2粉末;
④通过分液漏斗向烧瓶中加入浓盐酸;
⑤用NaOH溶液吸收多余的氯气;
⑥用向上排空气法收集氯气.
其中正确的操作顺序是 .
(2)烧瓶中发生反应的化学方程式是: .
(3)制得的氯气可选用 来干燥,烧杯中发生反应的离子方程式是 .
(4)在实验室里,常用加热食盐晶体和浓硫酸的混合物的方法来制取HCl,HCl是一种无色有刺激性气味的气体,密度比空气大,极易溶于水,它的水溶液叫氢氯酸,即盐酸
①实验室制取HCl的发生装置可选用制 的发生装置(填O2、Cl2、CO2中的一种).
②收集氯化氢气体时应采用 法.
③实验室可用 试纸放在瓶口检验HCl是否充满了集气瓶.
④图2哪些装置可作为多余氯化氢的吸收装置? .
查看习题详情和答案>>
(1)某同学进行实验时可能有如下操作:

①连接好装置并检查气密性
②缓缓加热;
③在烧瓶里加入MnO2粉末;
④通过分液漏斗向烧瓶中加入浓盐酸;
⑤用NaOH溶液吸收多余的氯气;
⑥用向上排空气法收集氯气.
其中正确的操作顺序是
(2)烧瓶中发生反应的化学方程式是:
(3)制得的氯气可选用
(4)在实验室里,常用加热食盐晶体和浓硫酸的混合物的方法来制取HCl,HCl是一种无色有刺激性气味的气体,密度比空气大,极易溶于水,它的水溶液叫氢氯酸,即盐酸
①实验室制取HCl的发生装置可选用制
②收集氯化氢气体时应采用
③实验室可用
④图2哪些装置可作为多余氯化氢的吸收装置?