题目内容
实验室制取并收集氯气的装置如图1:(1)某同学进行实验时可能有如下操作:

①连接好装置并检查气密性
②缓缓加热;
③在烧瓶里加入MnO2粉末;
④通过分液漏斗向烧瓶中加入浓盐酸;
⑤用NaOH溶液吸收多余的氯气;
⑥用向上排空气法收集氯气.
其中正确的操作顺序是
(2)烧瓶中发生反应的化学方程式是:
(3)制得的氯气可选用
(4)在实验室里,常用加热食盐晶体和浓硫酸的混合物的方法来制取HCl,HCl是一种无色有刺激性气味的气体,密度比空气大,极易溶于水,它的水溶液叫氢氯酸,即盐酸
①实验室制取HCl的发生装置可选用制
②收集氯化氢气体时应采用
③实验室可用
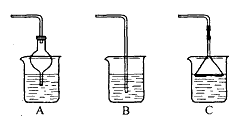
④图2哪些装置可作为多余氯化氢的吸收装置?
分析:(1)按照先连接装置检查气密性、装入药品、开始加热产生氯气、收集氯气、尾气处理的顺序进行排序;
(2)根据实验室制取氯气的反应原理写出反应的化学方程式;
(3)氯气不与硫酸反应,可以使用浓硫酸进行干燥;氯气有毒,可以使用氢氧化钠溶液吸收多余的氯气;
(4)①根据信息可知,制取氯化氢反应中,反应装置为固液加热装置,据此进行判断;
②氯化氢密度大于空气,应该采用向上排空气法收集;
③氯化氢溶于水,溶液显示酸性,可以使用湿润的蓝色石蕊试纸检验氯化氢气体;
④氯化氢极易溶于水,吸收氯化氢杂质应该使用放倒吸装置.
(2)根据实验室制取氯气的反应原理写出反应的化学方程式;
(3)氯气不与硫酸反应,可以使用浓硫酸进行干燥;氯气有毒,可以使用氢氧化钠溶液吸收多余的氯气;
(4)①根据信息可知,制取氯化氢反应中,反应装置为固液加热装置,据此进行判断;
②氯化氢密度大于空气,应该采用向上排空气法收集;
③氯化氢溶于水,溶液显示酸性,可以使用湿润的蓝色石蕊试纸检验氯化氢气体;
④氯化氢极易溶于水,吸收氯化氢杂质应该使用放倒吸装置.
解答:解:(1)先选取装置并连接装置、检查装置气密性,然后分别加入药品二氧化锰、浓盐酸,加热烧瓶使反应开始,收集氯气,对尾气进行称量,按照以上顺序进行排序为:①③④②⑥⑤,
故答案为:①③④②⑥⑤;
(2)实验室用二氧化锰与浓盐酸加热反应制取氯气,反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(3)氯化氢与浓硫酸不发生反应,通常使用浓硫酸干燥氯气;氯气与氢氧化钠溶液反应,所以多余的氯气可以使用氢氧化钠溶液吸收,
故答案为:浓硫酸;Cl2+2NaOH=NaCl+NaClO+H2O;
(4)①常用加热食盐晶体和浓硫酸的混合物的方法来制取HCl,反应装置与制取氯气反应装置相同;而制取氧气利用的是加热高锰酸钾固体、制取二氧化碳利用的是碳酸钙与盐酸反应,反应不需要放热,故验室制取HCl的发生装置可选用制氯气的发生装置,故答案为:Cl2;
②氯化氢的密度大于空气,不与空气成分反应,所以可以使用向上排空气法收集氯气,故答案为:向上排空气;
③氯化氢溶液为酸性溶液,检验氯化氢气体可以使用湿润的蓝色石蕊试纸,故答案为:湿润的蓝色石蕊;
④氯化氢极易溶于水,尾气吸收时应该采用防止倒吸装置,所以正确的装置为AC,故答案为:AC.
故答案为:①③④②⑥⑤;
(2)实验室用二氧化锰与浓盐酸加热反应制取氯气,反应的化学方程式为:MnO2+4HCl(浓)
| ||
故答案为:MnO2+4HCl(浓)
| ||
(3)氯化氢与浓硫酸不发生反应,通常使用浓硫酸干燥氯气;氯气与氢氧化钠溶液反应,所以多余的氯气可以使用氢氧化钠溶液吸收,
故答案为:浓硫酸;Cl2+2NaOH=NaCl+NaClO+H2O;
(4)①常用加热食盐晶体和浓硫酸的混合物的方法来制取HCl,反应装置与制取氯气反应装置相同;而制取氧气利用的是加热高锰酸钾固体、制取二氧化碳利用的是碳酸钙与盐酸反应,反应不需要放热,故验室制取HCl的发生装置可选用制氯气的发生装置,故答案为:Cl2;
②氯化氢的密度大于空气,不与空气成分反应,所以可以使用向上排空气法收集氯气,故答案为:向上排空气;
③氯化氢溶液为酸性溶液,检验氯化氢气体可以使用湿润的蓝色石蕊试纸,故答案为:湿润的蓝色石蕊;
④氯化氢极易溶于水,尾气吸收时应该采用防止倒吸装置,所以正确的装置为AC,故答案为:AC.
点评:本题考查了氯气的实验室制法、氯化氢的制法,题目难度中等,注意掌握实验室中常见气体的制取原理及装置选择,注意尾气吸收时,易溶于水的气体应该采用防止倒吸装置.

练习册系列答案
相关题目