摘要:3.溶液的蒸干:有些盐如FeCl3 MgCl2.由溶液蒸干得到晶体时.必须在蒸发过程中不断通入HCl气体.以抑制水解.
网址:http://m.1010jiajiao.com/timu_id_189501[举报]
(2012?天津模拟)A、B、C、D、E是中学化学常见的5种化合物,其中A、B是氧化物,单质X、Y是生活中常见的金属,试剂1和试剂2分别为常见的酸或碱.相关物质间的转化关系如下图所示(部分反应物与产物已略去):

请回答:
(1)①组成单质X的元素原子结构示意图是
 ;
;
②组成单质Y的元素在周期表中的位置
(2)若试剂1为强碱溶液,则X与试剂1反应的离子方程式是
(3)①若试剂1和试剂2相同,且E溶液加热蒸干并灼烧后可得到A,则A的化学式是
②将物质C溶于水,其溶液呈
(4)若试剂2为稀硫酸,工业上以E、稀硫酸和NaNO2为原料制备高效净水剂Y(OH)SO4,且反应中有NO生成,写出该反应的化学方程式
(5)请将D+Y→E的过程设计成一个能产生持续而稳定电流的原电池装置(使用盐桥),在框格内画出实验装置图,并在图中标出电极和试剂的名称.
查看习题详情和答案>>

请回答:
(1)①组成单质X的元素原子结构示意图是


②组成单质Y的元素在周期表中的位置
第四周期第 VIII族
第四周期第 VIII族
.(2)若试剂1为强碱溶液,则X与试剂1反应的离子方程式是
2Al+2H2O+2OH-=2AlO2-+3H2↑
2Al+2H2O+2OH-=2AlO2-+3H2↑
.(3)①若试剂1和试剂2相同,且E溶液加热蒸干并灼烧后可得到A,则A的化学式是
Fe2O3
Fe2O3
.②将物质C溶于水,其溶液呈
酸性
酸性
(填“酸性”、“中性”或“碱性”),原因用离子方程式可表示为Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.(4)若试剂2为稀硫酸,工业上以E、稀硫酸和NaNO2为原料制备高效净水剂Y(OH)SO4,且反应中有NO生成,写出该反应的化学方程式
2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑
2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑
.(5)请将D+Y→E的过程设计成一个能产生持续而稳定电流的原电池装置(使用盐桥),在框格内画出实验装置图,并在图中标出电极和试剂的名称.
 (1)将反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计成原电池其装置如图.电极X的材料是
(1)将反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计成原电池其装置如图.电极X的材料是Cu
Cu
;乙池中电极反应为2Ag++2e-=2Ag
2Ag++2e-=2Ag
;外电路中的电子流向Ag
Ag
电极.(2)取出盐桥后,电流计的指针
不能
不能
(填“能”或“不能”)发生偏转.(3)若甲、乙溶液反应前均为100mL,1mol/L.当外电路中转移0.02mol电子时,理论上X极的质量将减少
0.64
0.64
g,将乙溶液全部蒸干灼烧,最后可得固体的质量为8.84
8.84
g.
A、B、C、D、E是中学化学常见的5种化合物,其中A、B是氧化物,单质X、Y是生活中常见的金属,试剂1和试剂2分别为常见的酸或碱.相关物质间的转化关系如下图所示(部分反应物与产物已略去):

请回答:
(1)①组成单质X的元素原子结构示意图是______;
②组成单质Y的元素在周期表中的位置______.
(2)若试剂1为强碱溶液,则X与试剂1反应的离子方程式是______.
(3)①若试剂1和试剂2相同,且E溶液加热蒸干并灼烧后可得到A,则A的化学式是______.
②将物质C溶于水,其溶液呈______(填“酸性”、“中性”或“碱性”),原因用离子方程式可表示为______.
(4)若试剂2为稀硫酸,工业上以E、稀硫酸和NaNO2为原料制备高效净水剂Y(OH)SO4,且反应中有NO生成,写出该反应的化学方程式______.
(5)请将D+Y→E的过程设计成一个能产生持续而稳定电流的原电池装置(使用盐桥),在框格内画出实验装置图,并在图中标出电极和试剂的名称.
查看习题详情和答案>>

请回答:
(1)①组成单质X的元素原子结构示意图是______;
②组成单质Y的元素在周期表中的位置______.
(2)若试剂1为强碱溶液,则X与试剂1反应的离子方程式是______.
(3)①若试剂1和试剂2相同,且E溶液加热蒸干并灼烧后可得到A,则A的化学式是______.
②将物质C溶于水,其溶液呈______(填“酸性”、“中性”或“碱性”),原因用离子方程式可表示为______.
(4)若试剂2为稀硫酸,工业上以E、稀硫酸和NaNO2为原料制备高效净水剂Y(OH)SO4,且反应中有NO生成,写出该反应的化学方程式______.
(5)请将D+Y→E的过程设计成一个能产生持续而稳定电流的原电池装置(使用盐桥),在框格内画出实验装置图,并在图中标出电极和试剂的名称.
查看习题详情和答案>>
某化工厂利用含铁的矿物质A制取水合盐G的流程如图所示。已知:B中氧元素的质量分数为30%,气体C是形成酸雨的污染物之一。

(1) A中主要成分的化学式可能为 (只写一种)。
(2)操作a过程中 (能、不能)将F溶液直接蒸干。
(3)确认F溶液中不含有Fe3+的方法是___________ ___。
(4)反应①中存在多种反应,请写出其中属于非氧化还原反应的离子方程式
___ ___。
(5)工业上反应C→D的化学方程式是_________ _____。
查看习题详情和答案>>
用粗盐(含Ca2+ 、Mg2+ 、SO42- 、CO32-和泥沙等杂质)制备医用级纯度的NaCl,并测定医用NaCl的百分含量。某化学研究性学习小组成员设计了如下实验步骤:
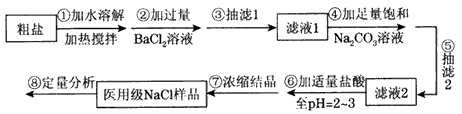
根据以上信息回答下列有关问题:
(1)步骤②中加入BaCl2溶液过量的原因:___________
(2)步骤③中抽滤装置如图,仪器C的名称:________;
(1)步骤②中加入BaCl2溶液过量的原因:___________
(2)步骤③中抽滤装置如图,仪器C的名称:________;
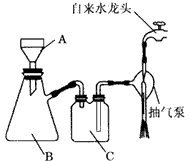
(3)若省略步骤“③抽滤1”后,能否通过步骤“⑤抽滤2”同时除去BaSO4和 CaCO3等沉淀,从沉淀溶解平衡的角度说明理由:____;
(4)步骤⑦浓缩与结晶操作时,当出现下列现象_________时,停止加热(填序号);
A.蒸发皿液面上出现极薄晶膜
B.蒸发皿底部刚出现细小晶粒
C.蒸发皿底部出现大量的晶体
D.蒸发皿中溶液全部蒸干
(5)取1.00 g干燥的医用级NaCl样品溶解于适量蒸馏水中,向其中加入含AgNO3 3.40 g的AgNO3溶液,Cl-即被完全沉淀。然后用Fe3+作指示剂,用NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以白色AgSCN沉淀的形式析出。
①滴定达到终点时,溶液呈红色,且半分钟内不褪色,写出表示该现象的离子方程式:____;
②在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果________(选填“偏高”“偏低”或“无影 响”)。
③若用0.100 mol·L-1 NH4SCN标准溶液滴定剩余的AgNO3时,用去上述浓度的NH4SCN溶液30.0 mL,则此医用级氯化钠样品中NaCl的百分含量为 ____。
查看习题详情和答案>>
(4)步骤⑦浓缩与结晶操作时,当出现下列现象_________时,停止加热(填序号);
A.蒸发皿液面上出现极薄晶膜
B.蒸发皿底部刚出现细小晶粒
C.蒸发皿底部出现大量的晶体
D.蒸发皿中溶液全部蒸干
(5)取1.00 g干燥的医用级NaCl样品溶解于适量蒸馏水中,向其中加入含AgNO3 3.40 g的AgNO3溶液,Cl-即被完全沉淀。然后用Fe3+作指示剂,用NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以白色AgSCN沉淀的形式析出。
①滴定达到终点时,溶液呈红色,且半分钟内不褪色,写出表示该现象的离子方程式:____;
②在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果________(选填“偏高”“偏低”或“无影 响”)。
③若用0.100 mol·L-1 NH4SCN标准溶液滴定剩余的AgNO3时,用去上述浓度的NH4SCN溶液30.0 mL,则此医用级氯化钠样品中NaCl的百分含量为 ____。