网址:http://m.1010jiajiao.com/timu_id_1753866[举报]
 目前工业上有一种方法是用CO2来生产燃料甲醇.为探究其反应原理,现进行如下实验,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2 (g)+3H2 (g)
目前工业上有一种方法是用CO2来生产燃料甲醇.为探究其反应原理,现进行如下实验,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2 (g)+3H2 (g) CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )
CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( ) 目前工业上有一种方法是用CO2来生产燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,为探究反应原理,现进行如下实验:
目前工业上有一种方法是用CO2来生产燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,为探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1mol CO2和4mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示.
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=
(2)该反应的平衡常数表达式为
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和4mol H2
(4)如果在相同的容器中事先充入1mol CH3OH和1mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为
目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
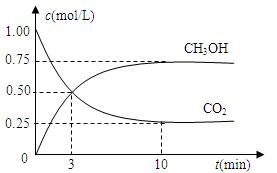
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1 mol CO2和4 mol H2
(4)如果在相同的容器中事先充入1 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
查看习题详情和答案>>目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1 mol CO2和4 molH2
(4)如果在相同的容器中事先充入1 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
查看习题详情和答案>>
目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1 mol CO2和4 mol H2 |
 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
查看习题详情和答案>>
mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
查看习题详情和答案>>