题目内容
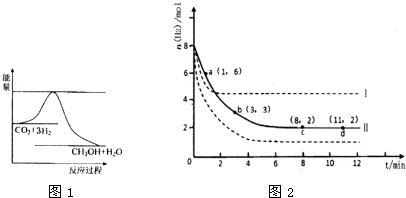
 目前工业上有一种方法是用CO2来生产燃料甲醇.为探究其反应原理,现进行如下实验,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2 (g)+3H2 (g)
目前工业上有一种方法是用CO2来生产燃料甲醇.为探究其反应原理,现进行如下实验,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2 (g)+3H2 (g) CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )
CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )分析:A、根据热化学方程式的含义和可逆反应的特征来回答;
B、根据反应速率v=
来计算回答;
C、根据等效平衡原理知识来回答;
D、根据化学平衡状态的标志:v(正)=v(逆)来判断.
B、根据反应速率v=
| △c |
| △t |
C、根据等效平衡原理知识来回答;
D、根据化学平衡状态的标志:v(正)=v(逆)来判断.
解答:解:A、2molCO2和6molH2反应达到平衡时,反应物不能进行彻底,所以放热小于73.5kJ,故A错误;
B、从反应开始到平衡,CO2的平均速率v(CO2)
=
=0.075mol/(L?S),故B错误;
C、再充入1molCO2和3molH2所建立的平衡和充入2mol CO2和6mol H2时的平衡是等效的,CO2的转化率不变,故C正确;
D、v(正)=v(逆)是化学平衡状态的标志,但是反应进行到3S时未达平衡,故D错误.
故选C.
B、从反应开始到平衡,CO2的平均速率v(CO2)
| △c |
| △t |
| 1mol/L-0.25mol/L |
| 10s |
C、再充入1molCO2和3molH2所建立的平衡和充入2mol CO2和6mol H2时的平衡是等效的,CO2的转化率不变,故C正确;
D、v(正)=v(逆)是化学平衡状态的标志,但是反应进行到3S时未达平衡,故D错误.
故选C.
点评:本题考查较为综合,涉及反应速率、热化学方程式的含义以及化学平衡移动原理知识,难度中等.

练习册系列答案
 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案
相关题目
 法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)
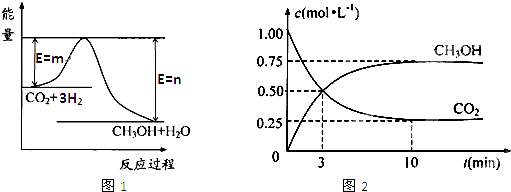
法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),如右上图表示该反应进行过程中能量(单位为kJ?mol-1)的变化.
CH3OH(g)+H2O(g),如右上图表示该反应进行过程中能量(单位为kJ?mol-1)的变化.
 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.