摘要:2.用0.1mo1/L盐酸分别跟20mL氢氯化钠溶液.20mL氨水反应.都消耗20mL盐酸.这说明氢氧化钠和氨水的关系是 A.离子浓度相同 B.PH相同 C.电离度相同 D.物质的量浓度相同
网址:http://m.1010jiajiao.com/timu_id_1753721[举报]
下列图示与对应的叙述相符的是( )
A、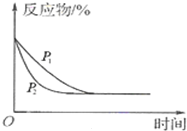 图表示压强对反应2A(g)+2B(g)═3C(g)+D(s)的影响,且P2>PI | B、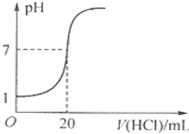 如图表示25℃时,用0.1 mol/L盐酸滴定20mL 0.1mol/L NaOH溶液,溶液的pH随加入盐酸体积的变化 | C、 依据如图,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH≈4 | D、 图中开关K置于A或B处均可以减缓铁的腐蚀 |
下列图像表达正确的是 ( )


A.图①表示25 ℃时,用0.1 mol/L盐酸滴定20 mL 0.1mol/L氨水
B.图②表示常温下,等量锌粉分别与两份足量的等体积等浓度的盐酸反应
C.图③表示向CaCl2溶液中通入CO2
D.图④表示向醋酸溶液中滴入氨水
查看习题详情和答案>>
下列图像表达正确的是 ( ) 

| A.图①表示25 ℃时,用0.1 mol/L盐酸滴定20 mL 0.1mol/L氨水 |
| B.图②表示常温下,等量锌粉分别与两份足量的等体积等浓度的盐酸反应 |
| C.图③表示向CaCl2溶液中通入CO2 |
| D.图④表示向醋酸溶液中滴入氨水 |
工业上常用漂白粉跟酸反应放出的氯气质量对漂白粉质量的百分比(x%)来表示漂白粉的优劣。漂白粉与酸的反应为:
Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2Cl2↑+2H2O
现为了测定一瓶漂白粉的x%,进行了如下实验。称取漂白粉样品2.
2Na2S2O3+I2=Na2S4O6+2NaI
滴定时用去Na2S2O3溶液20.0mL。试由上述数据计算该漂白粉的x%。
查看习题详情和答案>>