题目内容
工业上常用漂白粉跟酸反应放出的氯气质量对漂白粉质量的百分比(x%)来表示漂白粉的优劣。漂白粉与酸的反应为:Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2Cl2↑+2H2O
现为了测定一瓶漂白粉的x%,进行了如下实验。称取漂白粉样品2.
2Na2S2O3+I2=Na2S4O6+2NaI
滴定时用去Na2S2O3溶液20.0mL。试由上述数据计算该漂白粉的x%。
反应中消耗的Na2S2O3为0.1×0.02=0.002(mol)
与之反应的I2为:1/2×0.002=0.001(mol)
因而Cl2亦为0.001mol
x%=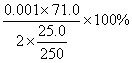 =35.5%
=35.5%
或列成一个总式:
x%=

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目