摘要:25.有100mL氯化镁和氯化铝的混合溶液.其中c(Mg2+)为0.1 mol·L-1.c(Cl-)为0.65 mol·L-1.要使Mg2+全部转化为沉淀分离出来.至少需加4 mol·L-1NaOH溶液的体积为 ( ) A.40 mL B.72 mL C.128 mL D.20 mL 第Ⅱ卷 非选择题
网址:http://m.1010jiajiao.com/timu_id_1752932[举报]
有100mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.1mol?L-1,c(Cl-)为0.65mol?L-1.要使Mg2+全部转化为沉淀分离出来,至少需加4mol?L-1NaOH溶液的体积为( )
查看习题详情和答案>>
有100mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.1mol?L-1,c(Cl-)为0.65mol?L-1.要使Mg2+全部转化为沉淀分离出来,至少需加4mol?L-1NaOH溶液的体积为( )
A.40 mL
B.72 mL
C.128 mL
D.20 mL
查看习题详情和答案>>
A.40 mL
B.72 mL
C.128 mL
D.20 mL
查看习题详情和答案>>
 工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.
工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.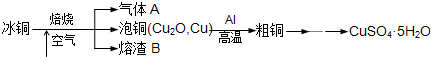
完成下列填空:
(1)气体A中的大气污染物可选用下列试剂中的
cd
cd
(填序号)吸收.a.浓H2SO4 b.浓HNO3
c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加
硫氰化钾
硫氰化钾
(填物质名称)溶液后呈红色,说明溶液中存在Fe3+,检验溶液中还存在Fe2+的方法是另取少量溶液,滴加几滴高锰酸钾的酸性溶液,紫色褪去,说明溶液中存在Fe2+
另取少量溶液,滴加几滴高锰酸钾的酸性溶液,紫色褪去,说明溶液中存在Fe2+
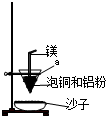
(注明试剂、现象).实验室可用如图的装置完成泡铜冶炼粗铜的反应.(3)泡铜冶炼粗铜的化学方程式是
3Cu2O+2Al
6Cu+Al2O3
| ||
3Cu2O+2Al
6Cu+Al2O3
.
| ||
(4)装置中镁带的作用是
燃烧放出大量的热,创造高温环境(或引燃剂)
燃烧放出大量的热,创造高温环境(或引燃剂)
.泡铜和铝粉混合物表面覆盖少量白色固体a,a是氯酸钾
氯酸钾
(填名称).沙子能否换成水?不能
不能
(填“能”或“不能”).(5)用滴定法测定CuSO4?5H2O的含量.取a g试样配成100mL溶液,取20.00mL用c mol/L (H2Y2-,滴定剂不与杂质反应)滴定至终点,消耗滴定剂bmL滴定反应:Cu2++H2Y2-?
| 滴定剂 |
| 5bc |
| 4a |
| 5bc |
| 4a |
(6)下列操作会导致CuSO4?5H2O含量的测定结果偏高的是
c
c
.a.滴定临近终点时,用洗瓶中的蒸馏水洗下滴定管尖嘴口的半滴标准液至锥形瓶中
b.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00mL进行滴定
c.滴定前,滴定管尖端有气泡,滴定后气泡消失.
(附加题)短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外第三层电子数目比第一层多1个,C-比A元素的离子多1个电子层,D元素的原子核外第二层比第一层多2个电子.回答下列问题:
(1)A、B、C、D四种元素的名称分别是
(2)C-的结构示意图为
 ;D元素在周期表中的位置是
;D元素在周期表中的位置是
(3)元素D的气态氢化物的电子式为
 ,其分子的结构特点是具有
,其分子的结构特点是具有
(4)工业上冶炼单质A的化学方程式为
(5)工业上常用单质B冶炼难熔的金属,写出氧化铁和单质B在高温下反应的化学方程式
(6)若将单质A、B用导线连接插入到氢氧化钠溶液中可以组成原电池,则正极材料是
查看习题详情和答案>>
(1)A、B、C、D四种元素的名称分别是
镁
镁
、铝
铝
、氯
氯
、碳
碳
;(2)C-的结构示意图为


第二周期、ⅣA
第二周期、ⅣA
;(3)元素D的气态氢化物的电子式为


正四面体
正四面体
结构,在一定条件下该氢化物可与单质C发生取代反应,若将等物质的量的该氢化物与单质C混合,在一定条件下充分反应后,生成物中物质的量最大的是HCl
HCl
(用化学式填写);(4)工业上冶炼单质A的化学方程式为
MgCl2(熔融)
Mg+Cl2↑
| ||
MgCl2(熔融)
Mg+Cl2↑
;
| ||
(5)工业上常用单质B冶炼难熔的金属,写出氧化铁和单质B在高温下反应的化学方程式
Fe2O3+2Al
Al2O3+3Fe
| ||
Fe2O3+2Al
Al2O3+3Fe
,该反应属于
| ||
放热
放热
反应(填“放热”或“吸热”),若反应中有0.25mol氧化铁参加反应,则消耗B单质的质量是13.5g
13.5g
,反应中转移电子的个数为9.03×1023
9.03×1023
;(6)若将单质A、B用导线连接插入到氢氧化钠溶液中可以组成原电池,则正极材料是
Mg
Mg
(用化学式填写),负极电极反应是2Al-6e-+8OH-=2AlO2-+3H2↑
2Al-6e-+8OH-=2AlO2-+3H2↑
.钠、镁、铝、铁等金属在日常生活、工业生产、航天事业中有着广泛的用途.
(1)4.8gAl在空气中放置一段时间之后,质量变为5.28g,则未发生变化的铝的质量为 g.
(2)向10mL 0.2mol/L的氯化铝溶液中逐滴加入未知浓度的氢氧化钡溶液,测得滴加10mL与滴加30mL时所得沉淀一样多.求氢氧化钡溶液的物质的量浓度.
(3)将镁、铝合金6.3g混合物加入到某浓度的硝酸中,产生标况下的气体8.96L(假设反应过程中还原产物是NO和NO2的混合气体),向所得溶液中加入氨水至沉淀达到最大量,沉淀干燥后测得的质量比原合金的质量增加10.2g,计算还原产物中NO和NO2的物质的量之比.
(4)现有一包铝热剂是铝粉和氧化铁粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(计算pH时假定溶液体积没有变化):①向其中一份固体中加入50mL 3.0mol/L的NaOH溶液,加热使其充分反应后过滤,测得滤液的c(OH-)为1.0mol/L;②向另一份固体中加入100mL 4.0mol/L的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)为0.2mol/L,计算这包铝热剂中铝的质量和氧化铁的质量.
查看习题详情和答案>>
(1)4.8gAl在空气中放置一段时间之后,质量变为5.28g,则未发生变化的铝的质量为
(2)向10mL 0.2mol/L的氯化铝溶液中逐滴加入未知浓度的氢氧化钡溶液,测得滴加10mL与滴加30mL时所得沉淀一样多.求氢氧化钡溶液的物质的量浓度.
(3)将镁、铝合金6.3g混合物加入到某浓度的硝酸中,产生标况下的气体8.96L(假设反应过程中还原产物是NO和NO2的混合气体),向所得溶液中加入氨水至沉淀达到最大量,沉淀干燥后测得的质量比原合金的质量增加10.2g,计算还原产物中NO和NO2的物质的量之比.
(4)现有一包铝热剂是铝粉和氧化铁粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(计算pH时假定溶液体积没有变化):①向其中一份固体中加入50mL 3.0mol/L的NaOH溶液,加热使其充分反应后过滤,测得滤液的c(OH-)为1.0mol/L;②向另一份固体中加入100mL 4.0mol/L的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)为0.2mol/L,计算这包铝热剂中铝的质量和氧化铁的质量.