摘要:7.将Fe片加到1L 0.5mol/L FeCL3溶液中.当Fe3+与Fe2+的浓度相等时.加入铁片的质量是( ) A. 2.8g B. 5.6g C.11.2g D.1.4g
网址:http://m.1010jiajiao.com/timu_id_1751956[举报]
几种短周期元素的原子半径及主要化合价见下表:
F与E的最高价氧化物对应水化物相互反应生成盐与水,分析上表的有关数据,并结合已学过知识,请用化学用语回答下列问题.
(1)写出C元素在周期表中的位置 .
(2)常温下这几种元素形成的单质能与水反应的有 .
(3)用电子式表示F2C的形成过程 .
(4)B、C、D最高价氧化物对应的水化物的酸性由大到小的顺序为 ,B、C、F的最高价氧化物对应的水化物形成溶液,浓度均为0.1mol/L时,pH由大到小的顺序为 .
(5)1molF2A2与水反应转移电子为 mol,反应生成的溶液与1L 0.5mol/L EB3溶液反应的离子方程式为 .
(6)将元素F的单质放入B与E形成的化合物的水溶液中,会产生气体和沉淀.若反应完全后生成标况下0.672L气体,则生成沉淀的最大质量为 g.
(7)F的同族元素M可以与G元素形成多种化合物,其中相对分子质量最小的分子为丙,其空间构型为正四面体型.用A的单质和丙可以制成原电池,电池中装有浓KOH溶液,用多孔的惰性电极浸入浓KOH溶液,在X极通入化合物丙,Y极通入A的单质,则X极是该电池的 极,X极的电极反应式为 .
查看习题详情和答案>>
| 元素代号 | A | B | C | D | E | F | G |
| 化合价 | -2 | -1 | -2、+6 | +4、-4 | +3 | +1 | +4、-4 |
| 原子半径(nm) | 0.074 | 0.099 | 0.102 | 0.117 | 0.143 | 0.186 | 0.077 |
(1)写出C元素在周期表中的位置
(2)常温下这几种元素形成的单质能与水反应的有
(3)用电子式表示F2C的形成过程
(4)B、C、D最高价氧化物对应的水化物的酸性由大到小的顺序为
(5)1molF2A2与水反应转移电子为
(6)将元素F的单质放入B与E形成的化合物的水溶液中,会产生气体和沉淀.若反应完全后生成标况下0.672L气体,则生成沉淀的最大质量为
(7)F的同族元素M可以与G元素形成多种化合物,其中相对分子质量最小的分子为丙,其空间构型为正四面体型.用A的单质和丙可以制成原电池,电池中装有浓KOH溶液,用多孔的惰性电极浸入浓KOH溶液,在X极通入化合物丙,Y极通入A的单质,则X极是该电池的
将K2SO4、(NH4)2SO4、NH4HCO3的固体混合物若干克加入到100mL 0.5mol/L的Ba(OH)2溶液中,共热使之充分反应,NH3全部逸出,同时生成沉淀8.6g。在所得固液混合物中加100mL 0.9mo/L的盐酸,沉淀部分溶解,同时生成448mL CO2气体(标准状况)。剩余盐酸用50mL 0.2mo/L的NaOH溶液恰好中和。求原混合物中各物质的质量。
查看习题详情和答案>>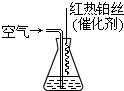 (2013?海淀区二模)氮化硅膜与二氧化硅膜相比较具有表面化学性能稳定等优点,故氮化硅膜可用于半导体工业.为生成氮化硅膜,可以用NH3和SiH4(硅烷)在一定条件下反应并在600℃的加热基板上生成氮化硅膜:
(2013?海淀区二模)氮化硅膜与二氧化硅膜相比较具有表面化学性能稳定等优点,故氮化硅膜可用于半导体工业.为生成氮化硅膜,可以用NH3和SiH4(硅烷)在一定条件下反应并在600℃的加热基板上生成氮化硅膜:3SiH4+4NH3
| ||
(1)以硅化镁为原料制备硅烷的反应和工业流程如下:
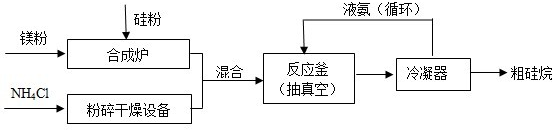
反应原理:4NH4Cl+Mg2Si
| ||
①NH4Cl的化学键类型有
极性键(或共价键)、离子键
极性键(或共价键)、离子键
,SiH4电子式为

②上述生产硅烷的过程中液氨的作用是
吸收热量,保证反应在常温下进行(答“制冷”或“降温”均可)
吸收热量,保证反应在常温下进行(答“制冷”或“降温”均可)
.③氨气也是重要的工业原料,写出氨气发生催化氧化反应生成NO的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
,实验室可利用如图所示装置完成该反应.
| ||
| △ |
在实验过程中,除观察到锥形瓶中产生红棕色气体外,还可观察到有白烟生成,白烟的主要成分是
NH4NO3(或:硝酸铵)
NH4NO3(或:硝酸铵)
.(2)三硅酸镁(Mg2Si3O8?nH2O)难溶于水,在医药上可做抗酸剂.它除了可以中和胃液中多余酸之外,生成的H2SiO3还可覆盖在有溃疡的胃表面,保护其不再受刺激.三硅酸镁与盐酸反应的化学方程式为
MgSi3O8?nH2O+4HCl═2MgCl2+3SiO2+(n+2)H2O
MgSi3O8?nH2O+4HCl═2MgCl2+3SiO2+(n+2)H2O
.将0.184g三硅酸镁加到50mL 0.1mol/L盐酸中,充分反应后,滤去沉淀,以甲基橙为指示剂,用0.1mol/L NaOH溶液滴定剩余的盐酸,消耗NaOH溶液30mL,则Mg2Si3O8?nH2O的n值为6
6
.(注:Mg2Si3O8的摩尔质量为260g/mol)