题目内容
将K2SO4、(NH4)2SO4、NH4HCO3的固体混合物若干克加入到100mL 0.5mol/L的Ba(OH)2溶液中,共热使之充分反应,NH3全部逸出,同时生成沉淀8.6g。在所得固液混合物中加100mL 0.9mo/L的盐酸,沉淀部分溶解,同时生成448mL CO2气体(标准状况)。剩余盐酸用50mL 0.2mo/L的NaOH溶液恰好中和。求原混合物中各物质的质量。
若Ba2+全部变为BaSO4,则其质量应为0.5mol/L×0.1L×233g/mol=11.65g,
若Ba2+全部变为BaCO3,则其质量应为0.5mol/L×0.1L×197g/mol=9.85g,
现有沉淀8.6g,比以上两数据都小,说明开始时Ba(OH)2过量,沉淀为BaSO4和BaCO3的混合物,共计8.6g。
设K2SO4、(NH4)2SO4、NH4HCO3物质的量分别为x、y、z,
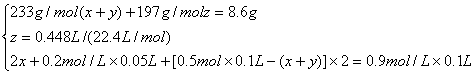
解得:![]()

练习册系列答案
相关题目