摘要:10.通常状况下.2molH2完全燃烧生成H2O(g)时放出484kJ热量.而生成H2O(l)时放出572kJ热量.则下列表达正确的是 ( ) A.H2的燃烧热:△H= -242 kJ·mol-1 B.2H2(g) + O2(g)=2H2O(g),△H= -242kJ·mol-1 C.H2O(g) =H2O (l),△H= +44 kJ·mol-1 D.H2O(l) =H2(g)+ 1/2O2(g),△H= +286kJ·mol-1
网址:http://m.1010jiajiao.com/timu_id_1751516[举报]
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)实验测得,在通常情况下,1gH2完全燃烧生成液态水,放出 142 . 9 kJ 热量。则H2燃烧的热化学方程式为
(2)用氢氧燃料电池进行下图所示实验。
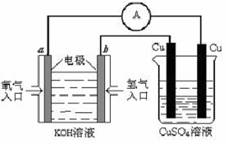
①氢氧燃料电池中,正极的电极反应式为
②上图装置中,某一铜电极的质量减轻3.2g,则a极上消耗的O2在标准状况下的体积
为 L
(3)用氢气是合成氨,反应的热化学方程式如下:
N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4KJ/mol
2NH3(g) △H=-92.4KJ/mol
① 下图表示合成氨反应达到平衡后,每次只改变温度、压强、催化剂中的某一条件,反应速率v与时间t的关系。其中表示平衡混合物中的NH3的含量最高的一段时间是 。图中t3时改变的条件可能是 。

②温度为T℃时,将4amolH2和2amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50。则反应的平衡常数为 。
查看习题详情和答案>>用NA代表阿伏加德罗常数,有关叙述中正确的是( )
| A、0.1mol钠在一定条件下与O2反应,当生成Na2O和Na2O2混合物时,失去的电子数为0.1NA | ||
| B、0.1mol Fe在一定条件下与O2反应,当生成FeO与Fe2O3混合物时,失去电子数为0.2NA | ||
C、标准状况下1L乙醇完全燃烧生成CO2分子数为
| ||
| D、常温、2.02×105Pa时1.6g氧气含有的原子数为0.2NA |
原子序数由小到大排列的四种短周期元素X、Y、Z、W,它们的原子序数之和为26,在同周期中W的原子半径最大,W和Z可形成W2Z和W2Z2;X、Y、Z三种元素中的任意两种之间可以组成甲、乙、丙…等许多种化合物.
(1)这四种元素的符号分别是X
 .
.
(2)甲是一种气体,通入紫色石蕊试液中,溶液变红.甲的分子式为
(3)乙是一种化石燃料,其分子呈正四面体构型,写出它的电子式
 ;560mL(标准状况下)乙完全燃烧生成液态水,产生热量22.25kJ.写出乙燃烧热的热化学方程式为
;560mL(标准状况下)乙完全燃烧生成液态水,产生热量22.25kJ.写出乙燃烧热的热化学方程式为
(4)丙是X和Z按原子个数比1:1组成的化合物.已知丙的溶液能使酸性高锰酸钾溶液褪色.将含有0.5mol丙的溶液滴加到100mL 2mol?L-1酸性高锰酸钾溶液中,溶液紫色恰好褪色.该反应的离子方程式为:
查看习题详情和答案>>
(1)这四种元素的符号分别是X
H
H
、YC
C
、ZO
O
、WNa
Na
,用电子式表示W2Z形成过程

(2)甲是一种气体,通入紫色石蕊试液中,溶液变红.甲的分子式为
CO2
CO2
,写出甲与W2Z2反应的化学方程式2CO2+2Na2O2=2Na2CO3+O2
2CO2+2Na2O2=2Na2CO3+O2
.(3)乙是一种化石燃料,其分子呈正四面体构型,写出它的电子式


CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═-890kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═-890kJ?mol-1
.(4)丙是X和Z按原子个数比1:1组成的化合物.已知丙的溶液能使酸性高锰酸钾溶液褪色.将含有0.5mol丙的溶液滴加到100mL 2mol?L-1酸性高锰酸钾溶液中,溶液紫色恰好褪色.该反应的离子方程式为:
2MnO4-+5H2O2+6H+=2Mn2++8H2O+502 ↑
2MnO4-+5H2O2+6H+=2Mn2++8H2O+502 ↑
.