摘要:11.某无色澄清溶液与NH4HCO3在一定条件下作用能产生气体.则在此溶液中肯定能大量共存的离子组是 ( ) A. MnO4-.Mg2+.Cl-.SO42- B.Na+.Ba2+.NO3-.SO42- C.Cl-.Na+.K+.SO42- D.K+.NO3-.SO42-.Al3+
网址:http://m.1010jiajiao.com/timu_id_1750754[举报]
澄清溶液与NH4HCO3在一定条件下作用能产生气体,下列各组离子中肯定不符合此条件的是
A.Fe3+ 、K+、H+ 、SO42-、 B.H+ 、Ba2+、NO3-、SO42-
C.Cl-、Ba2+ 、NO3-、OH- D.K+、NO3-、SO42-、Al3+
查看习题详情和答案>>
某无色澄清溶液与NH4HCO3作用能产生气体,则在此溶液中肯定能大量共存的离子组是( )
A.Cl-、Na+、K+、![]() B.Na+、Ba2+、
B.Na+、Ba2+、![]() 、
、![]()
C. ![]() 、Mg2+、Cl-、
、Mg2+、Cl-、![]() D.K+、
D.K+、![]() 、
、![]() 、Al3+
、Al3+
某无色澄清溶液与铝反应放出氢气,试分别情况在溶液中就可能大量存在的离子中H+、Zn2+、Na+、K+、OH-、SO42-、Cl-、CO32-、NO3-,按题目要求分成两组溶液:
第一组:两种阳离子___________,两种阴离子___________;
第二组:两种阳离子___________,三种阴离子_________________。
查看习题详情和答案>>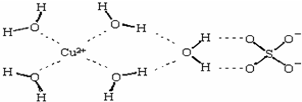 第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.
第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.(1)Cr的核外电子排布式为
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
;(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:图中虚线表示的作用力为
氢键、配位键
氢键、配位键
;(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4?H2O晶体.在Cu(NH3)4SO4?H2O晶体中,[Cu(NH3)4]2+ 为平面正方形结构,则呈正四面体结构的原子团是
SO42-
SO42-
,该原子团中心原子的杂化轨道类型是sp3
sp3
;(4)在一定条件下,Cu+比Cu2+稳定,请解释其原因:
Cu+基态离子的价电子排布为3d10,Cu2+基态离子的价电子排布为3d9,前者为半充满,所以Cu+比Cu2+稳定
Cu+基态离子的价电子排布为3d10,Cu2+基态离子的价电子排布为3d9,前者为半充满,所以Cu+比Cu2+稳定
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型.试推测四羰基镍的晶体类型是
分子晶体
分子晶体
,Ni(CO)4易溶于BC
BC
.A.水 B.四氯化碳 C.苯 D.硫酸镍溶液.
(2010?青岛二模)【化学-物质结构与性质】
第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.
(1)Cr的核外电子排布式为
(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:

图中虚线表示的作用力为
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4?H2O晶体.在Cu(NH3)4SO4?H2O晶体中,[Cu(NH3)4]2+ 为平面正方形结构,则呈正四面体结构的原子团是
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型.试推测四羰基镍的晶体类型是
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液.
查看习题详情和答案>>
第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.
(1)Cr的核外电子排布式为
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
;(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:

图中虚线表示的作用力为
氢键、配位键
氢键、配位键
;(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4?H2O晶体.在Cu(NH3)4SO4?H2O晶体中,[Cu(NH3)4]2+ 为平面正方形结构,则呈正四面体结构的原子团是
SO42一
SO42一
,其中心原子的杂化轨道类型是sp3
sp3
;(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型.试推测四羰基镍的晶体类型是
分子晶体
分子晶体
,Ni(CO)4 易溶于下列BC
BC
.A.水 B.四氯化碳 C.苯 D.硫酸镍溶液.