网址:http://m.1010jiajiao.com/timu_id_1750431[举报]
在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )。
zC(g),图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )。
A.200 ℃时,反应从开始到平衡的平均速率v(B)=0.02 mol·L-1·min-1
B.由图乙可知,反应xA(g)+yB(g)??zC(g)的ΔH<0,且a=2
C.若在图甲所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆)
D.200 ℃时,向容器中充入2 mol A和1 mol B,达到平衡时,A的体积分数小于0.5
(1)判断反应达到平衡状态的依据是
a. 生成CH3OH的速率与消耗CO的速率相等
b. 混合气体的密度不变
c. 混合气体的总物质的量不变
d. CH3OH、CO、H2的浓度都不再发生变化
(2)CO在不同温度下的平衡转化率与压强的关系如图1

①该反应△H
②实际生产条件控制在250℃、1.3×104 kPa左右,选择此压强的理由是
(3)右图2表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A
(4)一定条件下,0.5mol甲醇蒸气完全燃烧生成二氧化碳气体和液态水,放出Q KJ的热量.写出该反应的热化学方程式
(5)图3是甲醇燃料电池(电解质溶液为KOH溶液)结构示意图,写出 a处电极上发生的电极反应式
(14分)工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:


(1)判断反应达到平衡状态的依据是(填字母序号,下同)__________。
A.生成 的速率与消耗 的速率与消耗 的速率相等 的速率相等 |
| B.混合气体的密度不变 |
| C.混合气体的相对平均分子质量不变 |
D. 、 、 、 、 的浓度都不再发生变化 的浓度都不再发生变化 |
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将
 和
和 充入
充入 的密闭容器中,充分反应后,达到平衡时测得
的密闭容器中,充分反应后,达到平衡时测得 ,则CO的转化率为__________,此时的温度为__________。
,则CO的转化率为__________,此时的温度为__________。(3)要提高CO的转化率,可以采取的措施是__________。
a. 升温 b. 加入催化剂 c. 增加CO的浓度
d. 恒容下加入
 使压强变大 e. 恒容下加入惰性气体使压强变大 f. 分离出甲醇
使压强变大 e. 恒容下加入惰性气体使压强变大 f. 分离出甲醇(4)在250℃时,某时刻测得该温度下的密闭容器中各物质的物质的量浓度见下表:
| CO |  |  |
| 0.5 mol·L—1 | 2mol·L—1 | 6mol·L—1 |
(5)如图1所示,甲为恒容密闭容器,乙为恒压密闭容器。在甲、乙两容器中分别充入等物质的量的H2和CO,使甲、乙两容器初始容积相等。在相同温度下发生上述反应,并维持反应过程中温度不变。已知甲容器中CO的转化率随时间变化的图像如图2所示,请在图2中画出乙容器中CO的转化率随时间变化的图像。
 查看习题详情和答案>>
查看习题详情和答案>>
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
CO(g) + 2H2(g)  CH3OH(g)
CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号,下同)__________。
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
E. 容器中气体的压强不再改变
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)。
|
温度 |
250℃ |
300℃ |
350℃ |
|
K |
2.041 |
0.270 |
0.012 |
①由表中数据判断该反应的△H__________0(填“>”、“="”" 或“<”);
②某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO) =" 0.2" mol/L,则CO的转化率为__________,此时的温度为__________。
(3)要提高CO的转化率,可以采取的措施是__________。
a. 升温 b. 加入催化剂
c. 增加CO的浓度 d. 恒容下加入H2使容器内压强变大
e. 分离出甲醇 f. 恒容下加入惰性气体使容器内压强变大
(4)在250℃时,某时刻测得该温度下的密闭容器中各物质的物质的量浓度见下表:
|
CO |
H2 |
CH3OH |
|
0.5 mol·L-1 |
2mol·L-1 |
6mol·L-1 |
此时反应的正、逆反应速率的关系是:v(正) v(逆)(填“>”、“="”" 或“<”)。
(5)如图1所示,甲为恒容密闭容器,乙为恒压密闭容器。在甲、乙两容器中分别充入等物质的量的H2和CO,使甲、乙两容器初始容积相等。在相同温度下发生上述反应,并维持反应过程中温度不变。在图2中标出甲、乙两容器中CO的转化率随时间变化的对应图像(在图2相应曲线右侧的框格中分别标注“甲”、“乙”)。
查看习题详情和答案>>
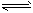 CH3OH(g) △H
CH3OH(g) △H(1)判断反应达到平衡状态的依据是(填字母序号,下 同)____。
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)。

②某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)= 0.2
mol/L,则CO的转化率为____,此时的温度为____。
(3)要提高CO的转化率,可以采取的措施是_________。
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2加压 e.加入惰性气体加压 f.分离出甲醇
(4)300℃时,在一定的压强下,5 mol CO与足量的H2在催化剂的作用下恰好完全反应变化的热量为454
kJ。在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
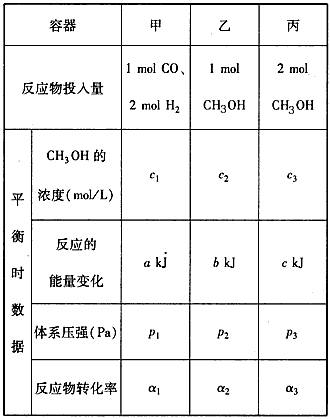
A.2c1>c3 B.a+b<90.8 C.2p2< p3 D.α1+α3<1