摘要:27.A.B.C.D.E.F.G.H是元素周期表中前四个周期的八种元素.已知A.C.E.G.H的基态原子中未成对电子数与其所在的周期序数相同.B与H同族.D.H.F 同一周期且原子序数依次增大.A与B的原子核外电子数之和与C原子的核外电子数相等且A.B.C能形成离子化合物.D原子的电子层数与价电子数相等但只有1个未成对电子.E的价电子数是G 的两倍.F原子的最外层也只有1个未成对电子. (1)B.C.D.H四种元素的第一电离能由大到小的顺序为 .电负性由小到大的顺序为 .B.F.G.H的最高价氧化物的水化物的酸性由强到弱的顺序为 (2)A.B.C形成的此化合物受热时发生反应的类型为 A.化合反应 B.分解反应 C.置换反应 D.氧化还原反应 (3)等质量的D的单质分别与足量的盐酸和氢氧化钠溶液反应放出的气体在常温常压下的体积比为 .将所得溶液混合时含有D元素的两种物质间发生反应的离子方程式为 . (4)G的最高价含氧酸的钠盐中属于酸式盐的一种的水溶液显 性.其原因是 (用必要的离子方程式和文字说明).溶液中离子浓度大小的顺序为 . (5)将E 与G的单质用导线连接同时插入氯化钠溶液中构成的原电池的总反应为 .E单质在常温下遇到A.B.C形成的另一化合物的浓溶液发生钝化现象.请写出过量的E 单质在此化合物的稀溶液中发生反应的离子方程式 .E3+与E2+的稳定性大小为 .E3+的基态电子排布式为 .在下图的方框内画出E的基态原子的轨道表示式.
网址:http://m.1010jiajiao.com/timu_id_1749272[举报]
A、B、C、D、E、F、G、H、I、J分别代表十种不同的有机物(其中A是化学工业重要原料之一).它们之间的相互转化关系如图: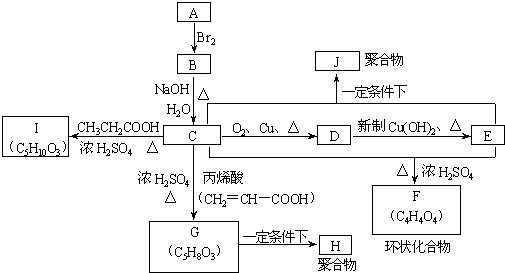
请回答下列问题:
(1)A的结构式简为
 ;指G→H的反应类型
;指G→H的反应类型
(2)写出下列转化的化学方程式.
①C→I
②C+E→J
(3)G有多种同分异构体,其中能与NaOH溶液及硫酸溶液均可反应;能发生银镜反应且生成的银与相应有机物的物质的量比为4:1,由符合条件的同分异构体数目有
查看习题详情和答案>>

请回答下列问题:
(1)A的结构式简为
CH2=CH2
CH2=CH2
;F的结构简式为

加聚反应
加聚反应
.(2)写出下列转化的化学方程式.
①C→I
CH3CH2COOH+HOCH2CH2OH
CH3CH2COOCH2CH2OH+H2O
| 浓硫酸 |
| △ |
CH3CH2COOH+HOCH2CH2OH
CH3CH2COOCH2CH2OH+H2O
| 浓硫酸 |
| △ |
②C+E→J
nCH2OHCH2CH2OH+nHOOCCOOH
 +(2n-1)H2O
+(2n-1)H2O
| 催化剂 |
 +(2n-1)H2O
+(2n-1)H2OnCH2OHCH2CH2OH+nHOOCCOOH
 +(2n-1)H2O
+(2n-1)H2O
| 催化剂 |
 +(2n-1)H2O
+(2n-1)H2O(3)G有多种同分异构体,其中能与NaOH溶液及硫酸溶液均可反应;能发生银镜反应且生成的银与相应有机物的物质的量比为4:1,由符合条件的同分异构体数目有
5
5
种,写出其中的一种同分异构体结构简式HCOOCH2CH2CH2CHO
HCOOCH2CH2CH2CHO
.A、B、C、D、E、F、G、H元素均属于短周期元素,它们在元素周期表中的位置关系如下表所示,已知D元素最高价氧化物对应的水化物的化学式为D(OH)3,该物质既能和强酸反应,也能和强碱反应.
(1)写出以下元素的元素符号 B
(2)写出F、G、H的最高价氧化物对应的水化物的化学式,并按酸性由弱到强的顺序排列:
(3)写出E、F、G的氢化物的化学式,并按稳定性由强到弱的顺序排列:
查看习题详情和答案>>
| A | E | |||||
| B | C | D | F | G | H |
Na
Na
DAl
Al
(2)写出F、G、H的最高价氧化物对应的水化物的化学式,并按酸性由弱到强的顺序排列:
H3PO4
H3PO4
<H2SO4
H2SO4
<HClO4
HClO4
(3)写出E、F、G的氢化物的化学式,并按稳定性由强到弱的顺序排列:
H2O
H2O
>H2S
H2S
>PH3
PH3
.A、B、C、D、E、F、G、H、I、J均为有机化合物.根据以下框图,回答问题:

(1)B和C均为有支链的有机化合物,B的结构简式为
(2)G 能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式
(3)写出:
⑤的化学方程式是
 .⑨的化学方程式是
.⑨的化学方程式是
 .
.
(4)①的反应类型是
(5)与H具有相同官能团的H的同分异构体的结构简式为
查看习题详情和答案>>

(1)B和C均为有支链的有机化合物,B的结构简式为
(CH3)2CHCOOH
(CH3)2CHCOOH
;C在浓硫酸作用下加热反应只能生成一种烯烃D,D的结构简式为(CH3)2C═CH2
(CH3)2C═CH2
.(2)G 能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式
CH2=C(CH3)-CHO
CH2=C(CH3)-CHO
.(3)写出:
⑤的化学方程式是




(4)①的反应类型是
水解反应
水解反应
,④的反应类型是取代反应
取代反应
,⑦的反应类型是氧化反应
氧化反应
.(5)与H具有相同官能团的H的同分异构体的结构简式为
CH2=CHCH2COOH和CH3CH=CHCOOH
CH2=CHCH2COOH和CH3CH=CHCOOH
.A、B、C、D、E、F、G、H、I是元素周期表前四周期的元素,它们在元素周期中的位置如图1所示:

(1)元素K的原子中未成对电子数是
(2)这些元素中第一电离能最大的是
(3)A、B、C三种元素形成的一种化合物叫三聚氰胺(结构如图2),由于其含氮量相当高被不法奶农添加到牛奶中来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石.三聚氰胺中二种环境的N原子的杂化形式分别是
(4)有下列物质①CA3;②GA3;③EH;④JH;⑤FD2.请将这些物质的熔点由高到低排列
查看习题详情和答案>>

(1)元素K的原子中未成对电子数是
3
3
个;(2)这些元素中第一电离能最大的是
Ar
Ar
(填写元素符号);G和H形成的每个原子均达到8电子稳定结构的化合物的分子式是PCl3
PCl3
;(3)A、B、C三种元素形成的一种化合物叫三聚氰胺(结构如图2),由于其含氮量相当高被不法奶农添加到牛奶中来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石.三聚氰胺中二种环境的N原子的杂化形式分别是
sp2、sp3
sp2、sp3
;该分子中位于同一平面的原子数最多是12
12
个;(4)有下列物质①CA3;②GA3;③EH;④JH;⑤FD2.请将这些物质的熔点由高到低排列
⑤>③>④>①>②
⑤>③>④>①>②
(填这些物质的序号)A、B、C、D、E、F、G、H是元素周期表中八种原子序数依次增大的短周期元素.
①A元素的原子半径在周期表中最小
②B元素的原子最外层电子数是次外层电子数的两倍
③C元素的最高价氧化物的水化物和氢化物反应生成盐
④D元素和E元素可以形成E2D、E2D2两种离子化合物
⑤G与D两种元素同主族,F、G、H三种元素同周期
⑥F元素是同周元素中离子半径最小的元素,H元素是同周期元素中原子半径最小的元素
(1)写出A、D、E三种元素形成的化合物的电子式 ;
(2)用惰性电极电解由E与H两元素形成的化合物的水溶液,其化学方程式为 ;
(3)八种元素中任意三种组成的易溶于水的酸性物质,能促进水电离的是 ,能抑制水电离的是 (各写一种化学式);
(4)某科研单位依据电化学原理用GD2来制备一种强酸R,装置如图,电极为含有某种催化剂的多孔材料,能吸附气体,同时也能使气体与电解质溶液充分接触.通入GD2的电极为 极,其电极反应式为 ;

(5)甲、乙、丙分别是B、F、G三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应产物不同.回答问题:
①向甲溶液中缓慢滴加过量的丙溶液,可观察到的实验现象是 ;
②向乙溶液中缓慢滴加过量的丙溶液发生反应的离子方程式为 、 .
查看习题详情和答案>>
①A元素的原子半径在周期表中最小
②B元素的原子最外层电子数是次外层电子数的两倍
③C元素的最高价氧化物的水化物和氢化物反应生成盐
④D元素和E元素可以形成E2D、E2D2两种离子化合物
⑤G与D两种元素同主族,F、G、H三种元素同周期
⑥F元素是同周元素中离子半径最小的元素,H元素是同周期元素中原子半径最小的元素
(1)写出A、D、E三种元素形成的化合物的电子式
(2)用惰性电极电解由E与H两元素形成的化合物的水溶液,其化学方程式为
(3)八种元素中任意三种组成的易溶于水的酸性物质,能促进水电离的是
(4)某科研单位依据电化学原理用GD2来制备一种强酸R,装置如图,电极为含有某种催化剂的多孔材料,能吸附气体,同时也能使气体与电解质溶液充分接触.通入GD2的电极为

(5)甲、乙、丙分别是B、F、G三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应产物不同.回答问题:
①向甲溶液中缓慢滴加过量的丙溶液,可观察到的实验现象是
②向乙溶液中缓慢滴加过量的丙溶液发生反应的离子方程式为