摘要:26.50ml 0.50mol·L-1盐酸和50ml 0.55mol·L-1烧碱在如下图所示的装置中进行中和反应.通过测定反应中所放出的热量可计算中和热,回答下列问题: (1)从实验装置上看.图中尚缺少的一种玻璃仪器是 (2)烧杯间填满碎泡沫塑料的作用是 (3)大烧杯如不盖硬纸板.求得中和热的数值将 (4)实验中改用60ml 0.50mol.L-1的盐酸跟50ml 0.50mol.L-1的烧碱溶液进行上述反应.与上述实验相比.所放出的热量 所求的中和热 简述理由 (5)若三次平行操作测得数据起始时盐酸与烧碱平均温度相同而终止温度与起始温度差(t2– t1)分别为①2.3℃②2.4℃③2.9℃.则最终代入计算式温度差平均为 ℃.
网址:http://m.1010jiajiao.com/timu_id_1748763[举报]
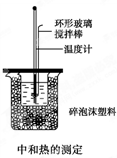 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:(1)烧杯间填满碎泡沫塑料的作用是
减小热量散失
减小热量散失
(2)大烧杯上如不盖硬纸板,求得的中和热数值
偏小
偏小
(填“偏大”“偏小”“无影响”).(3)实验中改用60mL 0.50mol?L-1盐酸进行反应,与上述实验相比,所放出的热量
不相等
不相等
(填“相等”、“不相等”),所求中和热相等
相等
(填“相等”、“不相等”),简述理由因中和热是指稀强酸与稀强碱发生中和反应生成1molH2O放出的热量,与酸碱的用量无关
因中和热是指稀强酸与稀强碱发生中和反应生成1molH2O放出的热量,与酸碱的用量无关
.(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会
偏小
偏小
(填“偏大”、“偏小”“无影响”).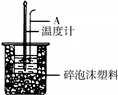 50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液在图所示的装置 中进行中和反应,通过测定反应过程中所放出的热量可计算反应热.
50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液在图所示的装置 中进行中和反应,通过测定反应过程中所放出的热量可计算反应热.(1)烧杯间填满泡沫塑料的作用是
减少实验过程中的热量损失;
减少实验过程中的热量损失;
;(2)大烧杯上若不盖硬纸板,求得的中和热数值
偏小
偏小
(填“偏大”、“偏小”、“无影响”)(3)如下图所示,仪器A的名称是
环形玻璃棒
环形玻璃棒
;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H>
>
-57.3KJ/mol(填“>”、“<”或“=”);(4)实验中改用80mL 0.50mol/L盐酸跟100mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
不相等
不相等
(填“相等、“不相等”),所求中和热
相等
相等
(填“相等、“不相等”).(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会
偏小
偏小
;(均填“偏大”、“偏小”、“无影响”)(6)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol·L-1的盐酸与50mL0.55mol·L-1的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题

(1)从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________________。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小'、“无影响”)
(3)实验中改用60mL 0.50mol·L-1的盐酸跟50mL 0.55mol·L-1的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是_______________________________;所求中和热的数值会________(填“相等”或 “不相等”),理由是______________________________。
查看习题详情和答案>>
(2)大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小'、“无影响”)
(3)实验中改用60mL 0.50mol·L-1的盐酸跟50mL 0.55mol·L-1的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是_______________________________;所求中和热的数值会________(填“相等”或 “不相等”),理由是______________________________。
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题

(1)从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________________。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3)实验中改用60 mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是_________________________________;所求中和热的数值会________(填“相等”或“不相等”),理由是___________________________。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
__________(填“偏大”、“偏小”、“无影响”)。
查看习题详情和答案>>
(2)大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3)实验中改用60 mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是_________________________________;所求中和热的数值会________(填“相等”或“不相等”),理由是___________________________。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
__________(填“偏大”、“偏小”、“无影响”)。
 (1)50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热,回答下列问题:①从实验装置上看,图中尚缺少的一种玻璃用品是
环形玻璃搅拌棒
环形玻璃搅拌棒
.②大烧杯上如不盖硬纸板,求得的中和热数值将
偏小
偏小
(填“偏大”“偏小”或“无影响”).(2)酸碱中和滴定是中学化学常见实验.
某学校化学课外小组用0.2000mol?L-1盐酸滴定未知浓度的氢氧化钠溶液,试回答下列问题.
①滴定过程中,眼睛应注视
锥形瓶内溶液颜色的变化
锥形瓶内溶液颜色的变化
.②在铁架台上垫一张白纸,其目的是
便于观察锥形瓶内液体颜色的变化,减小滴定误差
便于观察锥形瓶内液体颜色的变化,减小滴定误差
.③根据下表数据,计算被测烧碱溶液的物质的量浓度是
0.4000
0.4000
mol?L-1.(保留四位有效数字)| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
a.观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果
偏高
偏高
.b.若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果
偏高
偏高
.