摘要:22. (1)请结合水的结构与性质.回答以下关于水的问题: ①水分子在特定条件下容易结合一个H+形成水合氢离子(H3O+).该过程中所形成的共价键为 . A.极性键 B.非极性键 C.配位键 D.氢键 在H3O+中.3个O-H键是 的. ②给水施加一个弱电场.可使其在常温常压下结冰.称为“热冰 .下列物质熔化时.克服的微粒间的作用与“热冰 熔化时所克服的作用类型完全相同的是 A.金刚石 B.干冰 C.食盐 D.固态氨 (2)金属铁的晶体在不同温度下有两种堆积方式.晶胞分别如下图所示.则体心立方晶胞和面心立方晶胞中实际含有的铁原子个数之比为 .铁原子的配位数(与一个原子等距离且距离最近的原子数)之比为 . (3)超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛.AlN晶体与金刚石类似(其晶胞结构如右图.其中空心球所示原子位于立方体的顶点或面心.实心球所示原子位于立方体内).每个Al原子与 个N原子相连.与同一个Al原子相连的N原子构成的空间构型为 . (4)AlN样品中常含有碳和A12O3杂质.为测定AlN的质量分数.称取10.00 g样品.加入足量的NaOH溶液.生成NaAlO2和NH3.生成的NH3恰好被75 mL 1 mol/L-1硫酸溶液吸收为硫酸铵.则样品中AlN的质量分数= .
网址:http://m.1010jiajiao.com/timu_id_1747605[举报]
[化学--物质结构与性质]
研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.
(1)C、Si、N元素的电负性由大到小的顺序是______.C60和金刚石都是碳的同素异形体,金刚石熔点高于C60的熔点,原因是______.
(2)A、B均为短周期金属元素.依据下表数据,写出B原子的电子排布式:______.
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,为d或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+______颜色(填“无”或“有”).
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.
①COCl2分子的结构式为 ,②COCl2分子内含有______(填标号);
,②COCl2分子内含有______(填标号);
A.4个σ键 B.2个σ键、2个π键
C.2个σ键、1个π键 D.3个σ键、1个π键
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是______.
查看习题详情和答案>>
研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.
(1)C、Si、N元素的电负性由大到小的顺序是______.C60和金刚石都是碳的同素异形体,金刚石熔点高于C60的熔点,原因是______.
(2)A、B均为短周期金属元素.依据下表数据,写出B原子的电子排布式:______.
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.
①COCl2分子的结构式为
A.4个σ键 B.2个σ键、2个π键
C.2个σ键、1个π键 D.3个σ键、1个π键
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是______.
查看习题详情和答案>>
研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是 .C60和金刚石都是碳的同素异形体,二者比较熔点高的是 ,原因是 .
(2)A为短周期金属元素,依据下表数据,写出A的基态原子的轨道表示式 .
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色.如[Cu(H2O)4]2+显蓝色.据此判断25号元素Mn,形成的[Mn(H2O)6]2+络合离子 (填“无”或“有”)颜色.
(4)H-C≡C-COOH分子内含有 个σ键, 个π键.其中碳原子釆取 杂化轨道方式.
(5)CO可以与金属铁形成配合物分子Fe(CO)5,Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)═Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是 .
查看习题详情和答案>>
(1)O、Si、N元素的电负性由大到小的顺序是
(2)A为短周期金属元素,依据下表数据,写出A的基态原子的轨道表示式
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
(4)H-C≡C-COOH分子内含有
(5)CO可以与金属铁形成配合物分子Fe(CO)5,Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)═Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
⑴O、Si、N元素的电负性由大到小的顺序是____________________。C60和金刚石都是碳的同素异形体,二者中熔点较高的是____________。
⑵A为短周期金属元素,依据下表数据,A的基态原子的轨道表示式为
________________________________。
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
⑷H-C≡C-COOH分子内含有的σ键、π键的个数依次为_______________,其中碳原子的杂化方式为___________________。
⑸CO可以与金属铁形成配合物分子Fe(CO)5。Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键的类型是______________。
⑹W元素的原子的M能层为全充满状态,且核外的未成对电子只有一个,W晶体中微粒的堆积方式是下图中 (选填“甲”、“乙”或“丙”);若W晶体中一个晶胞的边长为a cm,则W晶体的密度为 (写出含a的表达式,用NA表示阿伏加德罗常数)。



甲 乙 丙 查看习题详情和答案>>
(8分)研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题。
(1)C、Si、N元素的电负性由大到小的顺序是__________________。
(2)A、B均为短周期金属元素。依据下表数据,写出B原子的电子排布式:______________。
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4[来源:学科网ZXXK] |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(4)利用CO可以合成化工原料COCl2。请判断COCl2分子内含有________。
A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3个σ键、1个π键 查看习题详情和答案>>
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N元素的电负性由大到小的顺序是 ,
C60和金刚石都是碳的同素异形体,二者相比,熔点高的是 ,原因是 。
(2)A、B均为短周期金属元素,依据表中数据,写出B的基态原子的电子排布式: 。
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
[Mn(H2O)6]2+ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为
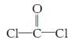 ,每个COCl2分子内含有 个σ键, 个π键,其中心原子采取 杂化轨道方式。
,每个COCl2分子内含有 个σ键, 个π键,其中心原子采取 杂化轨道方式。②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)。反应过程中,断裂的化学键只有配位键,则形成的化学键类型是 。 查看习题详情和答案>>