网址:http://m.1010jiajiao.com/timu_id_1747230[举报]
①M的原子结构示意图为
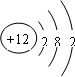

②以M、Al为电极,KOH溶液为电解质溶液,则负极的电极反应式为
(2)淬火是将金属工件加热到某温度,随即浸入淬冷介质中快速冷却的金属热处理工艺.
①使用水进行淬火,若生成磁性氧化铁,该反应的化学方程式为
| ||
| ||
②验证铁用水淬火后的固体产物是否存在+3价的铁,可选用的试剂为
A.H2O2溶液B.铜粉C.稀硫酸D.KMnO4溶液
(3)高铁酸钾在水中的反应为4Fe
2- 4 |
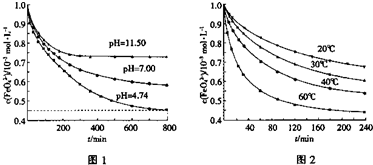
①图1是25℃时K2FeO4在不同pH溶液中浓度的变化情况.pH=4.74时,反应从开 始到800min的平均反应速率v(FeO
2- 4 |
②图1在800min后,三种溶液中K2FeO4的浓度均不再改变.观察图1判断随着pH 变大,此反应的平衡常数
③图2在240min后,四种溶液中K2FeO4的浓度均不再改变,则上述反应的反应热△H
(1)元素M是短周期元素,其常量存在于海水中,单质被誉为“国防金属”。
①M的原子结构示意图为______。
②以M、Al为电极,KOH溶液为电解质溶液,则负极的电极反应式为______。
(2)淬火是将金属工件加热到某温度,随即浸入淬冷介质中快速冷却的金属热处理工艺。
①使用水进行淬火,若生成磁性氧化铁,该反应的化学方程式为____________
②验证铁用水淬火后的固体产物是否存在+3价的铁,可选用的试剂为_______ (填序号)
A.H2O2溶液 B.铜粉 C.稀硫酸 D.KMnO4溶液
(3)髙铁酸钾在水中的反应为4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2
4Fe(OH)3+8OH—+3O2
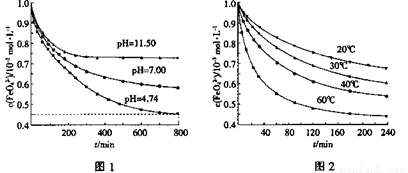
①图1是25℃时K2FeO4在不同pH溶液中浓度的变化情况。pH =4.74时,反应从开始到800min的平均反应速率v(FeO42—)=______ (保留两位有效数字)。
②图1在800min后,三种溶液中K2FeO4的浓度均不再改变。观察图1判断随着pH 变大,此反应的平衡常数______(填“变大”、“变小”或“不变”)。
③图2在240min后,四种溶液中K2FeO4的浓度均不再改变,则上述反应的反应热 △H______0(填“>”、“<”、“=”)。
查看习题详情和答案>>
(1)25℃时,某NaCl溶液中c(Cl–)=1×10-4 mol·L–1,则该溶液中c(Na+)∶c(OH-)=
(2)25℃时,将0.1 mol·L–1NaOH溶液与0.06 mol·L–1的H2SO4溶液等体积混合(忽略混合后体积的变化),求所得溶液的pH= 。25℃时,pH值为8的NaOH溶液与pH值为10的NaOH溶液等体积混合后,溶液中氢离子浓度最接近 。
(3)25℃时,下列四种溶液中,①pH=0的盐酸 ②0.1 mol·L–1的盐酸 ③0.01 mol·L–1的NaOH溶液 ④pH=11的NaOH溶液,由水电离生成氢离子浓度之比①︰②︰③︰④是: (填字母)
A.1︰10︰100︰1000 B.0︰1︰12︰11
C.14︰13︰12︰11 D.14︰13︰2︰3
(4)某温度(t℃)时,测得0.01mol·L-1 的NaOH溶液的pH=11,
①则该温度下水的Kw= 。
②在该温度下测得某溶液pH=3,则该溶液中c(H+)∶c(OH- )=________。
③该温度下将pH=2的盐酸和pH=11的氢氧化钠溶液等体积混合,pH=______________
(5) 纯水中c(H+)=5.0×10–7 mol·L–1,则此时纯水中的c(OH–) = ;若温度不变,滴入稀硫酸使c(H+)=5.0×10–3 mol·L–1,则c(OH–) = ;在该温度时,往水中滴入NaOH溶液,溶液中的c(OH–)=5.0×10–2 mol·L–1,则溶液中c(H+)= 。
查看习题详情和答案>>
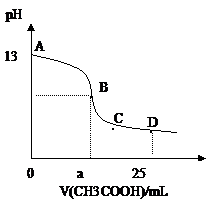 A.B点的横座标a==12.5,且有c(Na+)==c(CH3COO—)
A.B点的横座标a==12.5,且有c(Na+)==c(CH3COO—) A.B点的横座标a==12.5,且有c(Na+)==c(CH3COO—)
A.B点的横座标a==12.5,且有c(Na+)==c(CH3COO—)