摘要:16.在密闭容器中的反应:N2(g)+3H2(g) 2NH3.在672K.30MPa下n(NH3)和n(H2) 随时间变化的关系如图所示.下列叙述正确的是 A.点a处的正反应速率比点b的大 B.点c点的正反应速率等于逆反应速率 C.点d (t1时刻)的n (N2)比点e (t2时刻)处的n (N2)大 D.其他条件不变.773k下反应至t1时刻.此时画出的两根平行间的距离将要变大
网址:http://m.1010jiajiao.com/timu_id_1747030[举报]
在密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应),在672K,30MPa下n(NH3)和n(H2) 随时间变化的关系如图所示。下列叙述正确的是
2NH3(g)(正反应为放热反应),在672K,30MPa下n(NH3)和n(H2) 随时间变化的关系如图所示。下列叙述正确的是

![]() A.点a处的正反应速率比点b的大
A.点a处的正反应速率比点b的大
![]() B.点c点的正反应速率等于逆反应速率
B.点c点的正反应速率等于逆反应速率
![]() C.点d (t1时刻)的n (N2)比点e (t2时刻)处的n (N2)大
C.点d (t1时刻)的n (N2)比点e (t2时刻)处的n (N2)大
![]() D.其他条件不变,773k下反应至t1时刻,此时画出的两根平行 间的距离将要变大
D.其他条件不变,773k下反应至t1时刻,此时画出的两根平行 间的距离将要变大
在密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应),在672K,30MPa下n(NH3)和n(H2)随时
2NH3(g)(正反应为放热反应),在672K,30MPa下n(NH3)和n(H2)随时
间变化的关系如图所示。下列叙述正确的是
A.点a处的正反应速率比点b的大
B.点c点的正反应速率等于逆反应速率
C.点d (t1时刻)的n (N2)比点e (t2时刻)处的n (N2)大
D.其他条件不变,773k下反应至t1时刻,此时画出的两根平行间的距离将要变大
查看习题详情和答案>>在密闭容器中,对于反应:N2(g)+3H2(g)?2NH3(g),在反应起始时N2和H2分别为1mol和3mol,当达到平衡时,N2的转化率为30%.若以NH3为起始反应物,反应条件与上述反应相同时,欲使其达到平衡时各成分的百分含量与前者相同,则NH3的起始物质的量和它的转化率,正确的是( )
查看习题详情和答案>>
在密闭容器中,使2molN2和6molH2混合发生反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应)下列说法错误的是( )
查看习题详情和答案>>
| A.升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量变大 |
| B.升高平衡体系的温度(保持体积不变),混合气体的密度不变 |
| C.当反应达到平衡时,N2和H2的浓度比是1:3 |
| D.当达到平衡时,充入氩气,并保持压强不变,平衡将逆向移动 |
已知:N2(g)+3H2(g) 2NH3(g)△H=
—92 kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
2NH3(g)△H=
—92 kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
|
|
H2(g) |
N2(g) |
NH3(g) |
|
1mol分子中的化学键形成时要释放出的能量/kJ |
436 |
946 |
a |
A.如图可表示合成氨过程中的能量变化
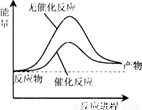
B.a的数值为391
C.Q1的数值为92
D.相同条件下,反应物若为2molN2和6molH2,放出热量Q2>2Q1
查看习题详情和答案>>