题目内容
已知:N2(g)+3H2(g) 2NH3(g)△H=
—92 kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
2NH3(g)△H=
—92 kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
|
|
H2(g) |
N2(g) |
NH3(g) |
|
1mol分子中的化学键形成时要释放出的能量/kJ |
436 |
946 |
a |
A.如图可表示合成氨过程中的能量变化
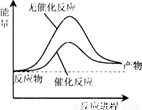
B.a的数值为391
C.Q1的数值为92
D.相同条件下,反应物若为2molN2和6molH2,放出热量Q2>2Q1
D
【解析】
试题分析:A.右图表示合成氨过程中在有、无催化剂时的反应途径的变化,错误。B,a的数值求解为: 2a +(946+3×436)=92,解得a=1173,错误。C。该反应是可逆反应,不能进行到底,故放出热量小于92,错误。D,增大反应物浓度平衡向正反应方向移动,放出热量大于原来的2倍。正确。
考点:考查反应途径、反应热可逆反应、外界条件对化学平衡的影响等知识。

已知 :N2(g)+3H2(g)  2NH3(g) ΔH=-92 kJ·mol-1。
2NH3(g) ΔH=-92 kJ·mol-1。
(1) 在500℃、2.02×107Pa和铁催化条件下2L密闭容器中充入1molN2和3mol H2,10 min时达到平衡,有0.2 mol NH3生成,则10 min内用氢气表示的该反应的平均速率v(H2)为 ,H2的转化率为__________。
(2)充分反应后,放出的热量______(填“<”“>”“=”)92.4kJ,理由是
 。
。
(3)为有效提高氢气的转化率,实际生产中宜采取的措施有____________
| A.降低温度 | B.不断补充氮气 | C.恒容下充入He来增大压强 |
| D.升高温度 E.原料气不断循环 F.及时移出氨 |



 (08福州市期末)已知反应N2(g)+3 H2(g) 2NH3(g),△H<0,向某体积恒定的密闭容器中按体积比l∶3充入N2和H2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图,Y可以是()
(08福州市期末)已知反应N2(g)+3 H2(g) 2NH3(g),△H<0,向某体积恒定的密闭容器中按体积比l∶3充入N2和H2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图,Y可以是()