网址:http://m.1010jiajiao.com/timu_id_1746393[举报]
(1)实验操作Ⅱ需加入适宜的试剂,你认为最好选用的试剂是
A.KMnO4(H+)溶液 B.硝酸 C.H2O2 D.浓硫酸
(2)操作V的离子方程式为
(3)图乙是操作Ⅵ、X制取无水FeCl3、AlCl3的部分装置(铁架台、加热装置等已略去).
①图乙中,装置a由
②循环物质A是
③装置b中填充的物质可以是
A.碱石灰 B.无水氯化钙 C.浓硫酸 D.五氧化二磷
(4)你认为该同学的实验最后

已知:AlCl3,FeCl3,分别在183℃、315℃升华
(1)在焙烧炉中发生反应:
①Fe2O3(S)+3C(s)
| 加热 |
②3CO(g)+Fe2O3(s)
| 加热 |
③反应2Fe2O3(s)+3C(s)
| 加热 |
(2)①Al2O3,Cl2和C在氯化炉中高温下发生反应,当生成1molAlCl3.时转移
| ||
| ||
②将AlCl3?6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的
①氧化性 ②吸水性 ③难挥发性 ④脱水性
a.只有①b.只有②c.只有②③d.只有②③④
(3)海洋灯塔电池是利用铝、石墨为电极材料,海水为电解质溶液,构成电池的其正极反应式
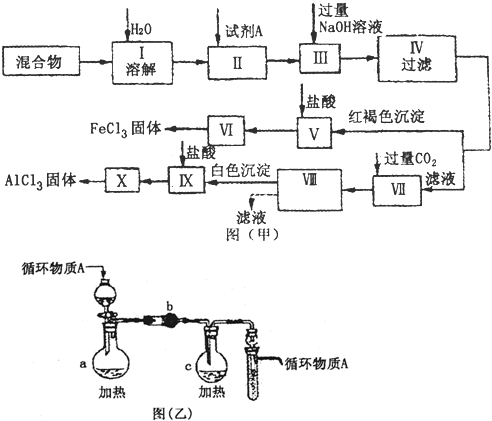
(12分)固体AlCl3和FeCl3混合物中含有少量FeCl2和Al2(SO4)3,某同学设计并进行实验对该混合物进行分离,以得到纯净的AlCl3和FeCl3,图甲是该同学设计并进行的实验:

(1)实验操作Ⅱ需加入适宜的试剂,你认为最好选用的试剂是___________。
A.KMnO4(H+)溶液 B.硝酸 C.H2O2 D.浓硫酸
(2)操作V的离子方程式为_______________________________________________;
操作Ⅶ的离子方程式为________________________________________________。
(3)图乙是操作Ⅵ、X制取无水FeCl3、AlCl3的部分装置(铁架台、加热装置等已略去)。

①图乙中,装置a由____________、圆底烧瓶、双孔塞和导管组成。
②循环物质A是______________________。
③装置b中填充的物质可以是_______________________(填编号)。
A.碱石灰 B.无水氯化钙 C.浓硫酸 D.五氧化二磷
(4)你认为该同学的实验最后_____________(填“能”或“不能”)得到纯净的AlCl3和FeCl3。若不能,请你完善该同学的实验步骤设计(用文字叙述):________________
_____________________________________________。(若能,此空不填)
查看习题详情和答案>>
(本小题18分)已知两个羧基之间在浓硫酸作用下脱去一分子水生成酸酐,如:

某酯类化合物A是广泛使用的塑料增塑剂。A在酸性条件下能够生成B、C、D。

(1) CH3COOOH称为过氧乙酸,写出它的一种用途_______________________。
(2)写出B+E→CH3COOOH+H2O的化学方程式_________________________。
(3)写出F的一种结构简式____________________________________。
(4)写出A的结构简式__________________________。
(5) 1molC分别和足量的金属Na、NaOH反应,消耗Na与NaOH物质的量之比是_____ 。
(6)写出D的结构简式__________________________。
查看习题详情和答案>>