题目内容
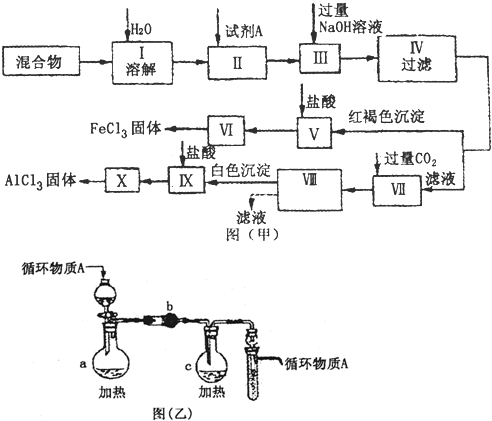
固体AlCl3和FeCl3混合物中含有少量FeCl2和Al2(SO4)3,某同学设计并进行实验对该混合物进行分离,以得到纯净的AlCl3和FeCl3,图甲是该同学设计并进行的实验:
(1)实验操作Ⅱ需加入适宜的试剂,你认为最好选用的试剂是 .
A.KMnO4(H+)溶液 B.硝酸 C.H2O2 D.浓硫酸
(2)操作V的离子方程式为 ;操作Ⅶ的离子方程式为 .
(3)图乙是操作Ⅵ、X制取无水FeCl3、AlCl3的部分装置(铁架台、加热装置等已略去).
①图乙中,装置a由 、圆底烧瓶、双孔塞和导管组成.
②循环物质A是 .
③装置b中填充的物质可以是 (填编号).
A.碱石灰 B.无水氯化钙 C.浓硫酸 D.五氧化二磷
(4)你认为该同学的实验最后 (填“能”或“不能”)得到纯净的AlCl3和FeCl3.若不能,请你完善该同学的实验步骤设计(用文字叙述): .(若能,此空不填)

(1)实验操作Ⅱ需加入适宜的试剂,你认为最好选用的试剂是
A.KMnO4(H+)溶液 B.硝酸 C.H2O2 D.浓硫酸
(2)操作V的离子方程式为
(3)图乙是操作Ⅵ、X制取无水FeCl3、AlCl3的部分装置(铁架台、加热装置等已略去).
①图乙中,装置a由
②循环物质A是
③装置b中填充的物质可以是
A.碱石灰 B.无水氯化钙 C.浓硫酸 D.五氧化二磷
(4)你认为该同学的实验最后
分析:由流程可知,混合物溶解后,加试剂A将亚铁离子氧化为铁离子,A为过氧化氢,然后加过量NaOH,过滤后得ⅤⅡ中含硫酸钠、偏铝酸钠,V为Fe(OH)3,Ⅵ为氯化铁溶液,Ⅶ中通入二氧化碳,得到的IX为Al(OH)3,X为氯化铝溶液,以此来解答.
解答:解:由流程可知,混合物溶解后,加试剂A将亚铁离子氧化为铁离子,A为过氧化氢,然后加过量NaOH,过滤后得ⅤⅡ中含硫酸钠、偏铝酸钠,V为Fe(OH)3,Ⅵ为氯化铁溶液,Ⅶ中通入二氧化碳,得到的IX为Al(OH)3,X为氯化铝溶液,
(1)由上述分析可知,氧化亚铁离子不能引入新杂质,只有C符合,故答案为:C;
(2)操作V中加盐酸,该离子方程式为3H++Fe(OH)3═Fe3+3H2O,操作Ⅶ通入二氧化碳,该离子方程式为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
故答案为:3H++Fe(OH)3═Fe3+3H2O;AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;
(3)图乙是操作Ⅵ、X制取无水FeCl3、AlCl3的部分装置,
①由图可知,a为分液漏斗,故答案为:分液漏斗;
②因FeCl3、AlCl3水解生成盐酸易挥发,应在通HCl气流中蒸发,则循环物质为HCl,故答案为:HCl;
③为干燥管,起干燥作用,应为固体干燥剂,且不与HCl反应,只有B、D符合,故答案为:BD;
(4)由流程可知,生成的沉淀没有洗涤,可能混有其它离子,则应在溶解沉淀前洗涤沉淀,所以不能得到纯净的AlCl3和FeCl3,
故答案为:不能;在溶解沉淀前洗涤沉淀.
(1)由上述分析可知,氧化亚铁离子不能引入新杂质,只有C符合,故答案为:C;
(2)操作V中加盐酸,该离子方程式为3H++Fe(OH)3═Fe3+3H2O,操作Ⅶ通入二氧化碳,该离子方程式为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
故答案为:3H++Fe(OH)3═Fe3+3H2O;AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;
(3)图乙是操作Ⅵ、X制取无水FeCl3、AlCl3的部分装置,
①由图可知,a为分液漏斗,故答案为:分液漏斗;
②因FeCl3、AlCl3水解生成盐酸易挥发,应在通HCl气流中蒸发,则循环物质为HCl,故答案为:HCl;
③为干燥管,起干燥作用,应为固体干燥剂,且不与HCl反应,只有B、D符合,故答案为:BD;
(4)由流程可知,生成的沉淀没有洗涤,可能混有其它离子,则应在溶解沉淀前洗涤沉淀,所以不能得到纯净的AlCl3和FeCl3,
故答案为:不能;在溶解沉淀前洗涤沉淀.
点评:本题考查物质的分离、提纯,把握流程中各步发生的反应及操作为解答的关键,注意过滤后的沉淀可能不纯及盐类水解应用,题目难度不大.

练习册系列答案
相关题目