摘要:13.将一定量的钠铝合金置于水中.合金全部溶解.得到20 mL pH=14的溶液.然后用1mol·L-1的盐酸溶液滴定.至沉淀质量最大时消耗盐酸40 mL.原合金中钠的质量为 ( ) A.0.92 g B.0.69 g C.0.46 g D.0.23 g 第Ⅱ卷 (1)请写出g元素在周期表中的位置 .并将铁的元素符号填在上图中合适的位置. (2)下列叙述正确的是 . A.氢化物Hd比Hh稳定.H2f的沸点高于H2O B.离子半径r C.化合物bh4与bf2均为非极性分子 D.由图中标出的8种元素形成的10e-结构的阳离子只有Na+和NH+4 (3)已知由元素a.b.w组成的化合物abw可称为“氢某酸 .分子中各原子均达到稳定状态.试写出其电子式 ,又知此酸对应的钾盐有剧毒.常温下其钾盐溶液的pH=9.则其溶液中由水电离出的c(OH-)= mol/L.该溶液中所有离子的浓度由大到小的顺序是 . (4)元素e的某化合物固体呈淡黄色.该物质与e2f的溶液反应生成淡黄色沉淀.则反应的离子方程式为 .
网址:http://m.1010jiajiao.com/timu_id_1745744[举报]
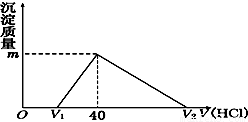
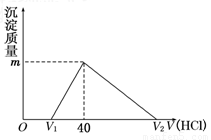
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
| A.原合金质量为0.92 g |
| B.标准状况下产生氢气896 mL |
| C.图中m值为1.56 g |
| D.图中V2为60 mL |
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
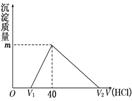
A.原合金质量为0.92 g
B.标准状况下产生氢气896 mL
C.图中m值为1.56 g
D.图中V2为60 mL
查看习题详情和答案>>
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1 mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
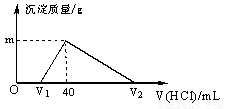
A.原合金质量为0.92 g
B.标准状况下产生氢气896 mL
C.图中m值为1.56
D.图中V2为60
查看习题详情和答案>>