题目内容
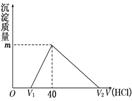
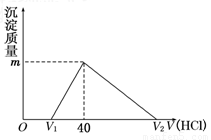
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1 mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
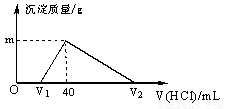
A.原合金质量为0.92 g
B.标准状况下产生氢气896 mL
C.图中m值为1.56
D.图中V2为60
【答案】
C
【解析】根据图像可知,氢氧化钠应该是过量的,过量的氢氧化钠是0.02mol,所以V1为20ml。因此与偏铝酸钠反应的盐酸是20ml,生成氢氧化铝是0.02mol,质量是1.56g,C正确。根据原子守恒可知金属铝的质量是0.02mol×27g/mol=0.54g。此时溶液中氯化钠是0.04mol,则金属钠的质量是0.92g,所以选项A不正确;生成氢气是0.03mol+0.02mol=0.05mol,标准状况下的体积是1.12,选项B不正确;溶解0.02mol氢氧化铝需要消耗0.06mol盐酸,所以图中V2为100,答案选C。

练习册系列答案
相关题目
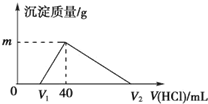 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL的溶液含NaOH 1mol/L,然后滴加1mol/L的盐酸,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL的溶液含NaOH 1mol/L,然后滴加1mol/L的盐酸,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )| A、原合金质量为0.92g | B、图中V2的值为60 | C、图中m的值为1.56 | D、产生氧气的体积为896mL(标准状况下) |
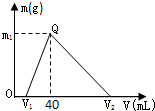 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200mL C(OH-)=0.1mol/L的溶液,然后逐滴加入1mol/L 的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,则下列说法正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200mL C(OH-)=0.1mol/L的溶液,然后逐滴加入1mol/L 的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,则下列说法正确的是( )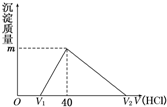 (2011?江西二模)将一定量的钠铝合金置于水中,合金全部溶解,得到20mL OH-浓度为1mol/L的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
(2011?江西二模)将一定量的钠铝合金置于水中,合金全部溶解,得到20mL OH-浓度为1mol/L的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )